题目内容
【题目】某校实验室有一无色澄清废液,其中除了硝酸钠以外,可能还含有氢氧化钠、碳酸钠、硫酸钠、硝酸钡中的一种或几种。
实验活动一:探究该废液的组成。取一定量的无色废液,进行如下图所示实验。

请回答下列问题:
(1)生成固体甲的化学方程式为_____________。
(2)原无色澄清废液中一定没有____________。
实验活动二:处理废液得到较纯净的硝酸钠溶液。将溶液A和原无色废液充分混合,无明显现象。接下来进行如下图所示实验。

(3)混合后废液中一定含有的溶质是(指示剂除外)__________,试剂①是___________。
【答案】CuSO4+Ba(NO3)2=Cu(NO3)2+BaSO4↓ Na2SO4、Na2CO3 NaNO3、Ba(NO3)2、Cu(NO3)2 Na2CO3或Na2CO3溶液
【解析】
(1)在实验活动一种,加酚酞试液后溶液呈红色,则证明溶液呈碱性。该无色澄清溶液中除了硝酸钠以外,可能还含有氢氧化钠、碳酸钠、硫酸钠、硝酸钡中的一种或几种。而且在加入硫酸铜溶液和过量的稀硝酸后,有固体甲产生,该固体只可能为硫酸钡,所以反应生成固体甲的化学方程式为:CuSO4+Ba(NO3)2=Cu(NO3)2+BaSO4↓。故答案为:CuSO4+Ba(NO3)2=Cu(NO3)2+BaSO4↓;
(2)由(1)可知,该无色溶液中含有硝酸钡,而碳酸钠、硫酸钠与硝酸钡不可共存。即原无色澄清废液中一定没有碳酸钠、硫酸钠。故答案为:Na2SO4、Na2CO3;
(3)由上述分析可知,原无色澄清废液中一定没有碳酸钠、硫酸钠,且原无色溶液呈碱性。在硝酸钠、氢氧化钠、硝酸钡中,只有氢氧化钠呈碱性,即原溶液中一定含有硝酸钠、氢氧化钠、硝酸钡。将溶液A和原无色废液充分混合,无明显现象,即不生成沉淀,溶液A的主要成分为H+、NO3-、Na+、Ca2+,其中H+会与氢氧化钠反应,则混合后废液中一定含有的溶质是硝酸钠、硝酸钡、硝酸铜;混合后溶液再加入过量氢氧化钠溶液后,杂质离子为OH-、Ba2+,且加入过量试剂①后会生成固体,为了除去杂质Ba2+且不引入新的杂质,试剂①应为碳酸钠或碳酸钠溶液。故答案为:NaNO3,Ba(NO3)2,Cu(NO3)2、Na2CO3或Na2CO3溶液。

【题目】分类、类比是初中化学常用的学习方法
|
|
|
|
A | B | C | D |
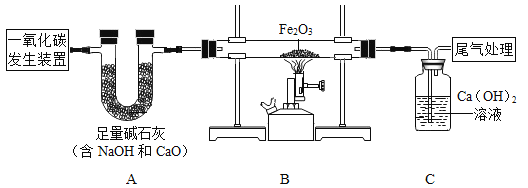
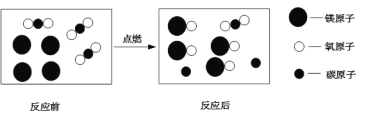
(1)初中化学有很多实验,若按照实验目的可将实验分为:探究物质组成的实验,探究物质反应前后质量关系的实验、物质检验的实验等,我们可以将实验中D与_____(填“A”或“B”或“C”)归为一类,分类依据是_____。
(2)学习了金属活动性顺序后,某同学通过查阅资料发现有下列反应:![]() ,
,![]() ,则在铁、镍、铜三种金属中,活动性最强的金属是_____,请运用类比的方法写出铝丝和氯化镍溶液反应的化学方程式_____。
,则在铁、镍、铜三种金属中,活动性最强的金属是_____,请运用类比的方法写出铝丝和氯化镍溶液反应的化学方程式_____。