题目内容
4.能源与我们的生活息息相关.(1)液化石油气(主要成分含有C4H10)是石油的产品,其完全燃烧的化学方程式为2C4H10+13O2$\frac{\underline{\;点燃\;}}{\;}$8CO2+10H2O.
(2)从表中的数据分析,与煤相比用天然气作燃料的优点是同质量煤和天然气燃烧,天然气放出热量更多.
| 1g物质完全燃烧 | ||
| 产生二氧化碳的质量/g | 放出的热量/kJ | |
| 甲烷 | 2.75 | 56 |
| 碳 | 3.67 | 32 |
(4)“安全意识“在我们心中共鸣.天然气(其密度小于空气)已在城乡普遍入户,为了及时发现漏气,可在厨房墙壁的上方安装报警器(填“上“或“下“).
分析 (1)根据反应物和生成物及其质量守恒定律可以书写化学方程式;
(2)根据从表数据分析,与煤相比,用天然气作燃料的优点有等质量的天然气和煤完全燃烧,天然气燃烧产生二氧化碳的质量小于煤,放出的热量高于煤进行解答;
(3)根据灭火的原理分析;
(4)天然气的主要成分是甲烷,甲烷的密度比空气小解答.
解答 解:
(1)液化石油气(主要成分含有C4H10)是石油的产品,其完全燃烧生成二氧化碳和水,化学方程式为:2C4H10+13O2$\frac{\underline{\;点燃\;}}{\;}$8CO2+10H2O;
(2)从表数据分析,与煤相比,用天然气作燃料的优点有等质量的天然气和煤完全燃烧,天然气燃烧产生二氧化碳的质量小于煤,放出的热量高于煤.
(3)用水灭火时,主要是水蒸发能收大量的热,能降低可燃物的温度至着火点以下;
(4)甲烷密度比空气密度小,为了及时发现漏气,可在厨房墙壁的上方安装报警器.
答案:
(1)2C4H10+13O2$\frac{\underline{\;点燃\;}}{\;}$8CO2+10H2O
(2)同质量煤和天然气燃烧,天然气放出热量更多
(3)使温度降低到着火点以下
(4)上
点评 解答本题要掌握化学方程式的书写方法和节能环保的重要性,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
14.逻辑推理是一种重要的化学思维方法,下列推理合理的是( )
| A. | 向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐 | |
| B. | 因为氧化物含有氧元素,所以含氧元素的化合物都是氧化物 | |
| C. | 通常盐是由金属阳离子和酸根阴离子构成的,硝酸铵中没有金属阳离子,不属于盐 | |
| D. | 因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳元素和氢元素 |
15.中小学生健康成长需要摄入足量的维生素.下列安徽地方特色品牌产品中维生素含量最丰富的是( )
| A. |  巢湖银鱼 | B. |  黄山臭桂鱼 | C. |  肥西老母鸡 | D. |  祁门猕猴桃 |
12.只用下列鉴别方法不能把待鉴别的物质区分开的是( )
| 待鉴别的物质 | 鉴别方法 | |
| A | 澄清石灰水和氢氧化钠溶液 | 加盐酸,观察现象 |
| B | 氯化铵固体和氢氧化钠固体 | 加熟石灰研磨,闻气味 |
| C | 生石灰和石灰石 | 加水,观察温度的变化 |
| D | 羊毛线和涤纶线 | 点燃,闻燃烧产生的气味 |
| A. | A | B. | B | C. | C | D. | D |
19.工业上常利用电石制乙炔气体(C2H2)时产生的灰浆和残渣制备化工原料KClO3和超细CaCO3.
(1)电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:
电石(CaC2)$\underset{\stackrel{\;}{→}}{水}$灰浆$\stackrel{露置于空气}{→}$残渣
其中电石与水反应生成氢氧化钙和乙炔,该反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑.残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如下:
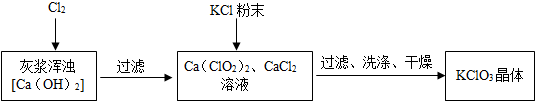
(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
上述流程中加入KCl粉末,KCl与Ca(ClO3)2(填化学式)发生了复分解反应,得到KClO3晶体.你认为能得到KClO3 晶体的原因是相同温度下,氯酸钾的溶解度小.
(4)洗涤时,可以选用下列BC作洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
过滤
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):
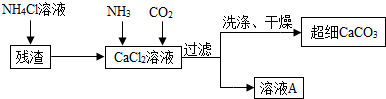
(5)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.
(1)电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:
电石(CaC2)$\underset{\stackrel{\;}{→}}{水}$灰浆$\stackrel{露置于空气}{→}$残渣
其中电石与水反应生成氢氧化钙和乙炔,该反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑.残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如下:

(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(4)洗涤时,可以选用下列BC作洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
过滤
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):

(5)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.
9.如表归类错误的是( )
| 选项 | 归类 | 物质(或元素) |
| A | 可燃性气体 | 氢气、一氧化碳、氧气 |
| B | 可溶性碱 | 氢氧 化钠、氢氧化钾、氢氧化钡 |
| C | 放热的化学反应 | 中和反应、生石灰与水反应 |
| D | 人体中常见微量元素 | 碘、锌、硒、铜等 |
| A. | A | B. | B | C. | C | D. | D |
16.下列物质的保存方式与空气成分无关的是( )
| A. | 真空包装食品 | B. | 在水中保存白磷 | ||
| C. | 密封保存浓盐酸 | D. | 密封保存氢氧化钠固体 |
14.下列物质的用途与性质不相对应的是( )
| A. | 高能燃料--氢气密度小 | |
| B. | 潜水员携带供氧设备--氧气能供给呼吸 | |
| C. | 人工降雨--干冰升华吸收大量的热 | |
| D. | 合金材料制造航天器--合金高强度、耐高温 |
