题目内容
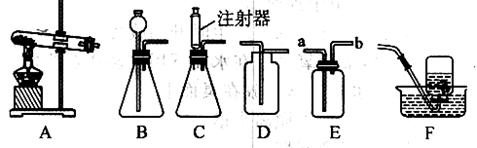
下图为某化学实验小组同学设计的制备氧气及探究可燃物燃烧条件的实验装置图。请回答下列问题:

(1)锥形瓶中发生的化学反应方程式为 _____________________________,
收集氧气可采取的方法是 _____________________________(写一种即可) 。
。
(2)实验时,可观察 到铜片上白磷燃烧而红磷未燃烧,说明可燃物燃烧需要满足的一个条件是 ____________________________。
到铜片上白磷燃烧而红磷未燃烧,说明可燃物燃烧需要满足的一个条件是 ____________________________。
将锥形瓶中生成的氧气通入烧杯并与杯底白磷接触时,观察到的现象是 __________________________________________。
【解析】本题考查气体的制取和燃烧条件的探究。
(1)过氧化氢在催化剂的作用下生成氧气和水;氧气密度比空气大且不易溶于水,可采用排水法或向上排空气法收集 。
。
(2)铜片上的白磷和红磷都与空气接触,且温度相同,但白磷能燃烧,红磷不燃烧,说明可燃物燃烧的条件之一是温度达到可燃物的着火点;向水中的白磷表面通入氧气时,白磷达到了燃烧的条件,在水中燃烧。
答案:(1)2H2O2 2H2O+O2↑ 排水法(或向上排空气法)
2H2O+O2↑ 排水法(或向上排空气法)
(2)温度要达到可燃物的着火点 白磷燃烧

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案在一个密闭的钢筒内有甲、乙、丙、丁四种物质,在电火花作用下,发生充分反应,测得反应前后各物质的质量如下:
| 甲 | 乙 | 丙 | 丁 | |
| 反应前质量/g | 64 | 10 | 1 | 25 |
| 反应后质量/g | 54 | 37 | 9 |
已知甲的相对分子质量为丁的2倍,则该反应的化学 方程式中甲与丁的化学计量数之比为( )
方程式中甲与丁的化学计量数之比为( )
A.1∶2 B.1∶1
C.2∶1 D.2∶3
下列有关过滤的说法,正确的是( )
|
| A. | 实验室过滤时要用到的所有仪器是:铁架台、酒精灯、漏斗、烧杯 |
|
| B. | 过滤时用玻璃棒轻轻搅动漏斗中的液体,以加快过滤速度 |
|
| C. | 用双氧水和二氧化锰制氧气,不再有氧气产生后所得的剩余物质可以用过滤方法分离 |
|
| D. | 可以用过滤方法使硬水软化 |
小煜同学通过学习知道,乙醇汽油是一种新型车用燃料,于是他对汽油中添加乙醇的目的进行了如下研究。
【猜想】猜想1:可以减少汽车尾气的污染;
猜想2:可以产生更多的热量,增强汽车的动力。
【设计与实验】
| 序号 | 实验步骤 | 实验现象 | 结论 |
| Ⅰ | 在两个蒸发皿中各加入10 mL冷水,控制相同燃烧条件,分别用乙醇和汽油作为燃料进行加热,记录从开始加热到水沸腾的时间 | 用乙醇加热耗时 118 s;用汽油加热耗时56 s | 猜想2______(填“成立”或 “不成立”) |
| Ⅱ | 实验Ⅰ停止加热后,取下蒸发皿,观察蒸发皿的底部 | 用乙醇加热的蒸发皿底部只有极少量炭黑,而用汽油加热的蒸发皿底部有大量炭黑 | ______(可仿照上格填写) |
【分析与讨论】(1)实验Ⅰ是一个对比实验,实验过程中不一定要控制的条件是________(填序号)。
A.水的初始温度必须相同
B.加热开始计时点必须相同
C.燃具产生火焰的大小必须相同
D.蒸发皿的大小必须相同
(2)汽车的发动机、排气管等部件易出现积炭,使用乙醇汽油后,这些部件产生的积炭量将________。
(3)目前乙醇汽油中乙醇的添加量约为10%,可一定程度节省石油资源。结合实验Ⅰ的结论分析,如果乙醇的添加量过大,会使汽车 动力________(填“增强”“减弱”或“不变”)。
动力________(填“增强”“减弱”或“不变”)。