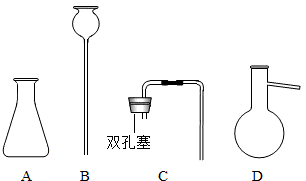
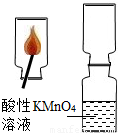
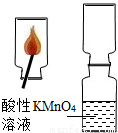
题目内容
小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出。迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失。
【查找资料】小钦从文献中查到:火柴头的主要成分为KClO3、硫磺粉(S)、三硫化二锑(Sb2S3)、玻璃粉等。
【提出猜想】猜想1:生成的二氧化碳气体使高锰酸钾溶液褪色
猜想2:生成的二氧化氮气体使高锰酸钾溶液褪色
猜想3:生成的二氧化![]() 硫气体使高锰酸钾溶液褪色
硫气体使高锰酸钾溶液褪色
小明从小钦查阅资料可以知道上述猜想 2错误,他的理由是:
【实验探究1】于是小明对猜想1进行了探究: 他在实验室制取二氧化碳,并将制得的CO2气体通入酸性高锰酸钾溶液中,发现酸性高锰酸钾溶液不褪色,他![]() 得出的结论是二氧化碳不会使高锰酸钾溶液褪色。
得出的结论是二氧化碳不会使高锰酸钾溶液褪色。
【实验探究2】SO2气体是否可使酸性高锰酸钾溶液褪色
在老师的指导下,小刘同学先制取了二氧化硫,探究SO2气体是否可以使酸性KMnO4溶液褪色。
| 操作步骤 | 实验现象 | 结论 |
|
|
【反思与评价】SO2气体可能是三硫化二锑(Sb2S3)与氧气反应得到,也可能是 得 到。
到。
反应物无氮元素,根据质量守恒定律,生成物一定无二氧化氮 表格中:将制取好的二氧化硫气体通入高锰酸钾溶液中
高锰酸钾溶液褪色 二氧化硫气体使高锰酸钾溶液褪色 猜想3正确
硫在氧气中燃烧

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
 小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.
小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.
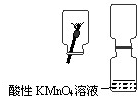 28、小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.
28、小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.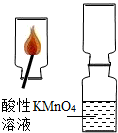 小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.
小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.