题目内容
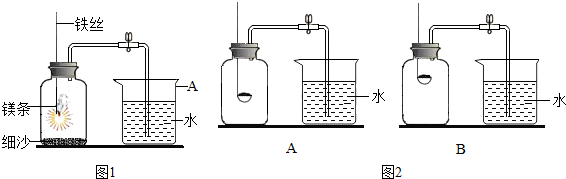
某校研究性学习小组用如图1装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
(1 )燃烧镁条,冷却后打开止水夹,水能进入集气瓶的原因是 .
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 %.现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气.
【发现问题】氮气是怎样减少的呢?
【假设一】氮气与镁条反应而减少.
【假设二】 .
【查阅资料】
镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体.镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁,后一反应的文字表达式是 .
【反思讨论】
①讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体.他们应该选择(填编号) . A.蜡烛 B.红磷 C.硫粉
②小组同学共同设计了如图2的两套装置,你认为合理的是(填编号) .
【实验拓展】
(3)小组的同学做完实验后又尝试用木炭或硫粉重新做了以上实验,发现水几乎没有进入集气瓶.经讨论,同学们一致认为如果事先在集气瓶内注入少量 溶液,实验也能取得较好的效果.
(4)反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是 .
(1 )燃烧镁条,冷却后打开止水夹,水能进入集气瓶的原因是
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的
【发现问题】氮气是怎样减少的呢?
【假设一】氮气与镁条反应而减少.
【假设二】
【查阅资料】
镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体.镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁,后一反应的文字表达式是
【反思讨论】
①讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体.他们应该选择(填编号)
②小组同学共同设计了如图2的两套装置,你认为合理的是(填编号)
【实验拓展】
(3)小组的同学做完实验后又尝试用木炭或硫粉重新做了以上实验,发现水几乎没有进入集气瓶.经讨论,同学们一致认为如果事先在集气瓶内注入少量
(4)反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是

考点:实验探究物质的性质或变化规律,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:由题目的信息可知:燃烧镁条,冷却后打开止水夹,水能进入集气瓶的原因是镁条与空气中的气体发生反应;如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%,因为氧气约占空气体积的21%;现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气,氮气减少的途径有:氮气与镁条反应而减少,氮气溶于水而减少等;选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体,他们应该选择红磷;小组同学共同设计了如图2的两套装置,我认为合理的是A,因为A能把空气中的氧气充分反应掉;木炭和氧气在点燃的条件下生成二氧化碳,硫粉与氧气在点燃的条件下生成二氧化硫,二氧化碳与二氧化硫都能被氢氧化钠溶液吸收.用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是:反应的药品只能与氧气反应,不与空气中的其它成分反应;生成物是固体,如果生成物中有气体,就要想办法把生成的气体吸收掉.
解答:解:(1)燃烧镁条,冷却后打开止水夹,水能进入集气瓶的原因是镁条与空气中的气体发生反应,故答案为:镁条与空气中的气体发生反应;
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%,因为氧气约占空气体积的21%;现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气,氮气减少的途径有:氮气与镁条反应而减少,氮气溶于水而减少等;镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体,他们应该选择红磷;小组同学共同设计了如图2的两套装置,我认为合理的是A,因为A能把空气中的氧气充分反应掉;故答案为:21;【假设二】氮气溶于水而减少;【查阅资料】镁+二氧化碳
碳+氧化镁;【反思讨论】B;A;
(3)木炭和氧气在点燃的条件下生成二氧化碳,硫粉与氧气在点燃的条件下生成二氧化硫,二氧化碳与二氧化硫都能被氢氧化钠溶液吸收;故答案为:氢氧化钠;
(4)用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是:反应的药品只能与氧气反应,不与空气中的其它成分反应;生成物是固体,如果生成物中有气体,就要想办法把生成的气体吸收掉;故答案为:反应的药品只能与氧气反应,不与空气中的其它成分反应;生成物是固体,如果生成物中有气体,就要想办法把生成的气体吸收掉;
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%,因为氧气约占空气体积的21%;现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气,氮气减少的途径有:氮气与镁条反应而减少,氮气溶于水而减少等;镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体,他们应该选择红磷;小组同学共同设计了如图2的两套装置,我认为合理的是A,因为A能把空气中的氧气充分反应掉;故答案为:21;【假设二】氮气溶于水而减少;【查阅资料】镁+二氧化碳
| 点燃 |
(3)木炭和氧气在点燃的条件下生成二氧化碳,硫粉与氧气在点燃的条件下生成二氧化硫,二氧化碳与二氧化硫都能被氢氧化钠溶液吸收;故答案为:氢氧化钠;
(4)用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是:反应的药品只能与氧气反应,不与空气中的其它成分反应;生成物是固体,如果生成物中有气体,就要想办法把生成的气体吸收掉;故答案为:反应的药品只能与氧气反应,不与空气中的其它成分反应;生成物是固体,如果生成物中有气体,就要想办法把生成的气体吸收掉;
点评:本考点属于实验方法和过程的探究,这类探究实验要具体问题具体分析,根据设计的步骤中不同的现象去思考、去探究,从而回答题目给出的问题.本考点主要出现在填空题和实验题中.

练习册系列答案
相关题目
关于下列三种粒子的说法中正确的是( )


| A、表示三种元素 |
| B、X表示阳离子 |
| C、都属于原子 |
| D、Z表示阴离子 |
通过下列实验得出的结论,其中正确的是( )

①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③既可说明水是由氢元素、氧元素组成,又说明了水分子中氢原子和氧原子个数之比
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低
⑤既可说明二氧化碳易溶于水,又说明了二氧化碳具有酸性.

①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③既可说明水是由氢元素、氧元素组成,又说明了水分子中氢原子和氧原子个数之比
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低
⑤既可说明二氧化碳易溶于水,又说明了二氧化碳具有酸性.
| A、①②③④ | B、②③④⑤ |
| C、②③④ | D、①②③④⑤ |
下列叙述正确的是( )
| A、原子核都是由质子和中子构成的 |
| B、在原子中,核内质子数和核外电子数不一定相等 |
| C、不同种类的原子,核内质子数不同,核外电子数可以相同 |
| D、原子里有相对较大的空间,电子在这个空间里做高速运动 |
 据报道,科学家已经研制出世界上最薄的材料-碳膜片,其厚度只有一根头发的二十分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成.下列有关碳膜片的说法中,正确的是( )
据报道,科学家已经研制出世界上最薄的材料-碳膜片,其厚度只有一根头发的二十分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成.下列有关碳膜片的说法中,正确的是( )| A、碳膜片属于单质 |
| B、碳膜片与C60是同一种物质 |
| C、碳膜片属于人工合成的有机化合物 |
| D、碳膜片在氧气中完全燃烧的产物和碳在氧气中完全燃烧的产物不同 |

 ,其中m表示
,其中m表示