题目内容
有NaOH和Na2CO3混合物l8.6 g.为测定其中NaOH的质量,将固体溶于水,并逐渐加入稀硫酸至100 g时,开始产生气体;再加入稀硫酸至100 g时,不再产生气体,生成气体共4.4 g
(提示:Na2CO3+H2SO4![]() Na2SO4+CO2↑+H2O)
Na2SO4+CO2↑+H2O)
(1)在下图中画出产生气体的质量与所加稀硫酸质量的关系曲线.
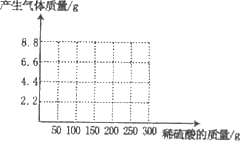
(2)求混合物中NaOH的质量是多少?
(3)所用稀硫酸的溶质质量分数是多少?
答案:
解析:
解析:
|
(1)如下图(1分)
解:(2)设混合物中Na2CO3的质量为x,100 g硫 酸溶液中H2SO4的质量为y. x=10.6 g(1分) y=9.8 g(1分) 混合物中氢氧化钠的质量为18.6 g-10.6 g=8.0 g(1分) (3)稀硫酸的溶质质量分数为:9.8 g/100 g×100%=9.8% (1分) |

练习册系列答案
相关题目
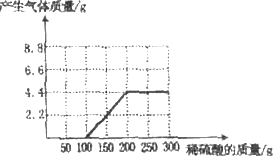
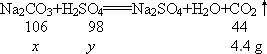
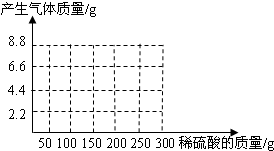 有NaOH和Na2CO3混合物l8.6g.为测定其中NaOH的质量,将固体溶于水,并逐渐加入稀硫酸至100g时,开始产生气体;再加入稀硫酸至100g时,不再产生气体,生成气体共4.4g
有NaOH和Na2CO3混合物l8.6g.为测定其中NaOH的质量,将固体溶于水,并逐渐加入稀硫酸至100g时,开始产生气体;再加入稀硫酸至100g时,不再产生气体,生成气体共4.4g

