题目内容
9.下列氧化物中,氧元素与另一元素的质量比是3:2的是( )| A. | CO2 | B. | CaO | C. | Fe2O3 | D. | SO3 |
分析 根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:A、CO2中氧元素与另一元素的质量比是(16×2):12=8:3,故选项错误.
B、CaO中氧元素与另一元素的质量比是16:40=2:5,故选项错误.
C、Fe2O3中氧元素与另一元素的质量比是(16×3):(56×2)=3:7,故选项错误.
D、SO3中氧元素与另一元素的质量比是(16×3):32=3:2,故选项正确.
故选:D.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
20.看见玉兔车金灿灿的车身后,小聪想到家里新换的水龙头.从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加.
【知识回放】
金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb (H) CuHg Ag Pt Au.
【作出猜想】
猜想1.Cr>Fe>Cu;
猜想2.Fe>Cu>Cr;
猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
【知识运用】
将铬片投入FeSO4溶液中,反应能否进行.若不能,写出理由;若能进行,请你写出反应的化学方程式Cr+FeSO4═CrSO4+Fe.
【知识回放】
金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb (H) CuHg Ag Pt Au.
【作出猜想】
猜想1.Cr>Fe>Cu;
猜想2.Fe>Cu>Cr;
猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 |  |  |  |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 铜片表面不产生气泡 |
将铬片投入FeSO4溶液中,反应能否进行.若不能,写出理由;若能进行,请你写出反应的化学方程式Cr+FeSO4═CrSO4+Fe.
17.下列各组日常生活中发生的变化,属于化学变化的是( )
| A. | 煤气燃烧 | B. | 瓷碗破碎 | C. | 胡萝卜雕花 | D. | 冰块熔化 |
14.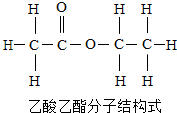 “酸”一词从有酸味的酒而来,国酒茅台窖存过程中产生的酸和酒中的醇缓慢反应生成有香味脂类物质,如乙酸乙酯,其分子结构见如图,下列有关乙酸乙酯的叙述正确的是( )
“酸”一词从有酸味的酒而来,国酒茅台窖存过程中产生的酸和酒中的醇缓慢反应生成有香味脂类物质,如乙酸乙酯,其分子结构见如图,下列有关乙酸乙酯的叙述正确的是( )
 “酸”一词从有酸味的酒而来,国酒茅台窖存过程中产生的酸和酒中的醇缓慢反应生成有香味脂类物质,如乙酸乙酯,其分子结构见如图,下列有关乙酸乙酯的叙述正确的是( )
“酸”一词从有酸味的酒而来,国酒茅台窖存过程中产生的酸和酒中的醇缓慢反应生成有香味脂类物质,如乙酸乙酯,其分子结构见如图,下列有关乙酸乙酯的叙述正确的是( )| A. | 乙酸乙酯分子有香味 | |
| B. | 乙酸乙酯分子是由4个碳原子、8个氢原子和2个氧原子构成 | |
| C. | 乙酸乙酯是由碳、氢、氧元素组成的化合物 | |
| D. | 乙酸乙酯中氢元素的质量分数最高 |
1. 等质量的M、N两种活泼金属,分别与足量的同质量分数的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是( )
等质量的M、N两种活泼金属,分别与足量的同质量分数的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是( )
 等质量的M、N两种活泼金属,分别与足量的同质量分数的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是( )
等质量的M、N两种活泼金属,分别与足量的同质量分数的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是( )| A. | 金属的活泼性N>M | B. | 两个反应生成H2的体积相等 | ||
| C. | 相对原子质量N>M | D. | 两个反应消耗盐酸的质量一定相等 |
18.请根据题意填写下表:
| ① | ② | ③ | ④ | |
| 化学符号 | ||||
| 表示意义 | 地壳中含量最高的金属元素与非金属元素形成的化合物 | 能保持水化学性质的微粒 | 二氧化硫中硫元素显+4价 | 两个碳酸根离子 |
 .
.
 铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是B
铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是B