题目内容
5. A、B、C、D、E、F分别是氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液、一氧化碳、二氧化碳中的一种.他们之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应,固态C物质可用于人工降雨.回答下列问题:
A、B、C、D、E、F分别是氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液、一氧化碳、二氧化碳中的一种.他们之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应,固态C物质可用于人工降雨.回答下列问题:(1)固态C物质俗称为干冰.
(2)E与F反应的实验现象为固体溶解,溶液由无色变成黄色.
(3)A与D反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(4)B能转化成A,反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
分析 二氧化碳的固体俗称干冰,升华时吸热,可以用作人工降雨;
二氧化碳能和氢氧化钠反应生成碳酸钠和水,能和氢氧化钙反应生成碳酸钙沉淀和水,氢氧化钙能和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,能和稀盐酸反应生成氯化钙和水,稀盐酸能和氧化铁反应生成氯化铁和水.
解答 解:二氧化碳的固体俗称干冰,升华时吸热,可以用作人工降雨;
二氧化碳能和氢氧化钠反应生成碳酸钠和水,能和氢氧化钙反应生成碳酸钙沉淀和水,氢氧化钙能和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,能和稀盐酸反应生成氯化钙和水,稀盐酸能和氧化铁反应生成氯化铁和水,因此A、B、C、D、E、F分别是碳酸钠、氢氧化钠、二氧化碳、氢氧化钙、稀盐酸和氧化铁;
(1)C物质是二氧化碳,俗称为干冰.
故填:干冰.
(2)稀盐酸能和氧化铁反应生成氯化铁和水,实验现象是固体溶解,溶液由无色变成黄色.
故填:固体溶解,溶液由无色变成黄色.
(3)氢氧化钙能和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故填:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(4)氢氧化钠能和二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O.
故填:2NaOH+CO2═Na2CO3+H2O.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.根据下表信息,完成表中空格:
| 化学符号 | 3Fe | 2N2 | Na+ | Al2O3 |
| 符号的意义 | 3个铁原子 | 2个氮分子 | 氯化钠溶液中的金属离子 | 铝元素与氧元素形成的化合物 |
20. 甲、乙、丙三种物质的溶解度曲线如图所示.下列叙述正确的是( )
甲、乙、丙三种物质的溶解度曲线如图所示.下列叙述正确的是( )
 甲、乙、丙三种物质的溶解度曲线如图所示.下列叙述正确的是( )
甲、乙、丙三种物质的溶解度曲线如图所示.下列叙述正确的是( )| A. | 40℃时,丙的溶解度最大 | |
| B. | 由60℃降温至40℃时,甲析出的晶体最多 | |
| C. | 40℃时,乙和丙的饱和溶液中溶质的质量分数相等 | |
| D. | 40℃时,100g水中加入50g丙,所得溶液中溶质的质量分数为33.3% |
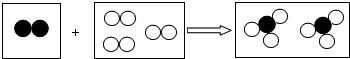
10.如图是某化学反应的微观模型,“ ”、“
”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
 ”、“
”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
| A. | 该反应属于分解反应 | |
| B. | 反应前后物质的化学性质发生变化 | |
| C. | 反应物和生成物中只有一种单质 | |
| D. | 参加反应的两种物质分子个数之比为2:3 |
