题目内容
先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加稀盐酸,可观察到红色逐渐消失,证明NaOH溶液与稀盐酸发生了化学反应.该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:NaOH溶液中滴入酚酞溶液,溶液变成了红色,过了一会儿红色就消失了.该小组对产生这种意外现象的原因作了如下猜想:①可能是酚酞溶液与空气中的氧气反应使红色消失;②可能是NaOH溶液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液.实验中“加热”和“滴入植物油”目的是 .实验结果表明酚酞溶液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论.
结论1:说明Na2CO3溶液呈 性;
结论2:说明酚酞溶液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:当NaOH溶液浓度很大时,就会出现上述意外现象.请设计方案证明上述取用的NaOH溶液浓度过大.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液.实验中“加热”和“滴入植物油”目的是
(2)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论.
结论1:说明Na2CO3溶液呈
结论2:说明酚酞溶液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:当NaOH溶液浓度很大时,就会出现上述意外现象.请设计方案证明上述取用的NaOH溶液浓度过大.
| 实验方法 | 实验现象 | 结论 |
| NaOH溶液浓度过大 |
考点:实验探究物质变化的条件和影响物质变化的因素,碱的化学性质,盐的化学性质
专题:科学探究
分析:可以根据溶液与酸碱指示剂相互作用时显色的情况进行分析、判断,从而得出正确的结论,氢氧化钠溶液呈碱性,pH>7,盐酸呈酸性,pH<7,氢氧化钠能与盐酸反应生成氯化钠,酚酞试液在碱性溶液中为红色.
解答:解:
(1)实验中“加热”和“滴入植物油”目的是:除去溶液中溶解的氧气;防止氧气进入氢氧化钠溶液.
(2)结论1.显碱性的物质能使酚酞试液变红色.碳酸钠溶液能使酚酞试液变红色,说明碳酸钠溶液显碱性.故填:碱.
(3)①实验方法:取两支试管,一支放入浓度大的NaOH溶液,另一支放入浓度小的NaOH溶液,分别滴入酚酞观察.
②实验现象:浓度大的试管不变红,浓度小的变红.
故答案为:
赶走溶液中少量的氧气,隔绝空气;碱;
(1)实验中“加热”和“滴入植物油”目的是:除去溶液中溶解的氧气;防止氧气进入氢氧化钠溶液.
(2)结论1.显碱性的物质能使酚酞试液变红色.碳酸钠溶液能使酚酞试液变红色,说明碳酸钠溶液显碱性.故填:碱.
(3)①实验方法:取两支试管,一支放入浓度大的NaOH溶液,另一支放入浓度小的NaOH溶液,分别滴入酚酞观察.
②实验现象:浓度大的试管不变红,浓度小的变红.
故答案为:
赶走溶液中少量的氧气,隔绝空气;碱;
| 实验方法 | 实验现象 | 结论 |
| 取两支试管,一支放入浓度大的NaOH溶液,另一支放入浓度小的NaOH溶液,分别滴入酚酞观察 | 浓度大的试管不变红,浓度小的变红 | NaOH溶液浓度过大 |
点评:本题主要考查了稀盐酸和氢氧化钠溶液发生中和反应及其设计实验进行相关方面证明等方面的内容,可以依据酸碱溶液的性质进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
今年央视3.15晚会曝光,少数不法厂家向液化石油气中掺入了二甲醚(C2H6O),二甲醚会对液化气罐的配件造成腐蚀,存在安全隐患.下列关于二甲醚的说法错误的是( )
| A、属于氧化物 |
| B、每个分子中含有9个原子 |
| C、碳、氢、氧元素的质量比为12:3:8 |
| D、碳元素的质量分数约为52.2% |
2012年3月7日澳大利亚遭遇严重洪灾,为防止灾后疾病传染,须对饮用水源进行处理,下列对净水措施的理解正确的是 ( )
| A、对水处理的合理顺序是:自然沉降→过滤→消毒→煮沸 |
| B、加入肥皂水可以将硬水软化 |
| C、过滤可以除去水中的一切杂质 |
| D、明矾净水的作用是消毒杀菌 |
区别下列物质所用试剂或方法不正确的是( )
| A、氮气与二氧化碳──燃着的木条 |
| B、蒸馏水与食盐水──蒸发 |
| C、空气与氧气──带火星的木条 |
| D、二氧化碳与氮气──石灰水 |
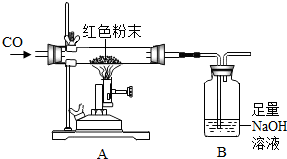 某化学兴趣小组.对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组.对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.