题目内容
7.请根据如图所示的实验过程和提供的数据,回答以下问题.
(1)100g溶液中含有的溶质有(用化学式表示).
(2)计算所得溶液A的溶质质量分数(写出计算过程,原子相对质量Na:23 C:12 O:16).
分析 (1)根据图示②中加入碳酸钠后又生成了气体,说明①中加入盐酸是过量的;即100g溶液中含有的溶质既有生成的氯化钠,又有过量的氯化氢;
(2)根据化学反应的方程式,结合溶质的质量分数计算公式来分析解答.
解答 解:(1)由图示②中加入碳酸钠后又生成了气体,说明①中加入盐酸是过量的;即100g溶液中含有的溶质既有碳酸钠与盐酸反应生成的氯化钠,又有过量的氯化氢;
(2)设②中加入的碳酸钠的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
106 44
x 2.2g
$\frac{106}{x}=\frac{44}{2.2g}$,
x=5.3g,
设,溶液A中氯化钠的质量为y,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
117 44
y 8.8g
$\frac{117}{y}=\frac{44}{8.8g}$
y=23.4g
溶液A的质量为:100g+5.3 g-2.2g=103.1g,
所得溶液A的溶质质量分数:$\frac{23.4g}{103.1g}$×100%=22.7%.
答:所得溶液A的溶质质量分数22.7%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
17.下列实验现象的描述中,不正确的是( )
| A. | 细铁丝在氧气中燃烧,火星四射,产生黑色固体 | |
| B. | 将氢氧化钠溶液滴入氯化铁溶液中,有红褐色沉淀产生 | |
| C. | 将二氧化碳通入紫色石蕊溶液中,溶液变为蓝色 | |
| D. | 将(NH4)2SO4和熟石灰混合研磨,有刺激性气味产生 |
18. 如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )
如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )
 如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )
如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )| A. | 葡萄汁能使紫色石蕊试液变蓝 | B. | 施用草木灰可以降低土壤碱性 | ||
| C. | 鸡蛋清的碱性比牙膏强 | D. | 胃酸过多的人不宜多食泡菜 |
15.下列变化属于物理变化的是( )
| A. | 氨水挥发 | B. | 铁锅生锈 | C. | 碳铵分解 | D. | 油米霉变 |
2.下列鉴别物质的试剂或方法,不正确的是( )
| 序 号 | 待鉴别的物质 | 鉴别试剂或方法 |
| A | 氯化钾与氯化铵固体 | 熟石灰、研磨 |
| B | 磷肥与钾肥 | 看外观(颜色) |
| C | 氢氧化钠溶液与碳酸钠溶液 | 酚酞溶液 |
| D | 聚乙烯与聚氯乙烯塑料 | 点燃闻气味 |
| A. | A | B. | B | C. | C | D. | D |
12.下列实验现象描述错误的是( )
| A. | 铁丝在氧气中燃烧火星四射 | |
| B. | 硫在氧气中燃烧产生蓝紫色火焰 | |
| C. | 红磷在氧气中燃烧产生白雾 | |
| D. | 铁丝浸入硫酸铜溶液表面有红色物质生成 |
16.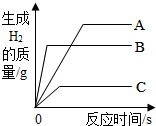 将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )(已知:A、B、C在生成物中均为+2价)
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )(已知:A、B、C在生成物中均为+2价)
 将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )(已知:A、B、C在生成物中均为+2价)
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )(已知:A、B、C在生成物中均为+2价)| A. | 消耗盐酸的质量是A>B>C | B. | 金属活动性顺序是A>B>C | ||
| C. | 反应速率由快到慢A>B>C | D. | 相对原子质量是A>B>C |

 (1)请从H、C、O、Cl、Na中选择适当的元素组成符合下列要求的物质的化学式:
(1)请从H、C、O、Cl、Na中选择适当的元素组成符合下列要求的物质的化学式: