题目内容
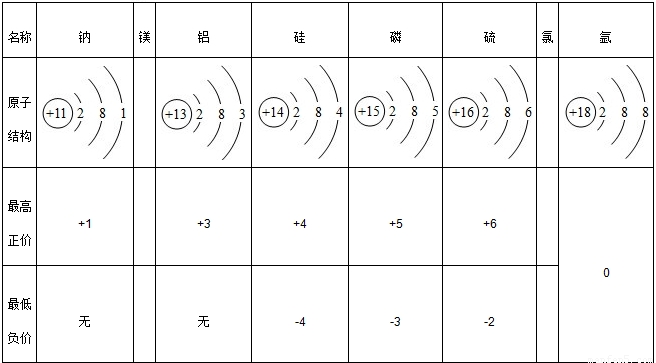
47、根据下表所给信息回答问题:
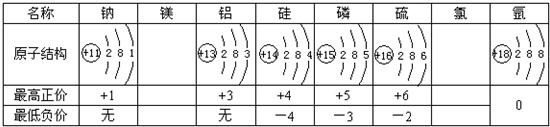
(1)按照上表中排列的递变规律,填写镁元素与氯元素相应的空格.
(2)上表中所有原子的
(3)除氩元素外,其他元素的最高正化合价等于
(4)非金属元素的负价数等于

(1)按照上表中排列的递变规律,填写镁元素与氯元素相应的空格.
(2)上表中所有原子的
电子层数
相同,从左到右,最外层电子数
、元素的最高正价数
均随核电荷数的递增而依次递增.(3)除氩元素外,其他元素的最高正化合价等于
最外层电子数
.(4)非金属元素的负价数等于
8减去最外层电子数
.分析:根据表中排列的递变规律:同一周期原子的最外层电子数从左到右逐渐增加;电子层数等于周期数;元素的最高正价数与元素原子的最外层电子数相同;进行解答本题.
解答:答:(1)根据表中排列的递变规律:同一周期原子的最外层电子数从左到右逐渐增加,可知:
镁元素原子结构示意图为: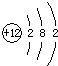 ;元素的最高正价数为:+2; 最低负价:无;
;元素的最高正价数为:+2; 最低负价:无;
氯元素原子结构示意图为: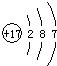 ;元素的最高正价数为:+7; 最低负价:-1;
;元素的最高正价数为:+7; 最低负价:-1;
故答案为: ;+2;无;
;+2;无; ;+7;-1;
;+7;-1;
(2)根据表中排列的递变规律可知:元素原子结构的电子层数相同;元素的最外层电子数从左向右逐渐递增;元素的最高正价数从左向右逐渐递增;
故答案为:电子层数相同;最外层电子数;元素的最高正价数;
(3)根据表中排列的递变规律可知:元素的最高正化合价等于最外层电子数,氩元素的最高正化合价等于0,
故答案为:最外层电子数;
(4)根据表中排列的递变规律可知:非金属元素的负价数等于8减去最外层电子数;
故答案为:8减去最外层电子数.
镁元素原子结构示意图为:
 ;元素的最高正价数为:+2; 最低负价:无;
;元素的最高正价数为:+2; 最低负价:无;氯元素原子结构示意图为:
 ;元素的最高正价数为:+7; 最低负价:-1;
;元素的最高正价数为:+7; 最低负价:-1;故答案为:
 ;+2;无;
;+2;无; ;+7;-1;
;+7;-1;(2)根据表中排列的递变规律可知:元素原子结构的电子层数相同;元素的最外层电子数从左向右逐渐递增;元素的最高正价数从左向右逐渐递增;
故答案为:电子层数相同;最外层电子数;元素的最高正价数;
(3)根据表中排列的递变规律可知:元素的最高正化合价等于最外层电子数,氩元素的最高正化合价等于0,
故答案为:最外层电子数;
(4)根据表中排列的递变规律可知:非金属元素的负价数等于8减去最外层电子数;
故答案为:8减去最外层电子数.
点评:信息题中往往有着共性信息,抽取出来用于直接解题很有必要.这类题目的应对策略应是阅读---理解---综合运用新原理,新方法完成任务.

练习册系列答案
相关题目
工业上的常说“三酸两碱”是重要的化工原料.实验室桌面上的五个试剂瓶内(如图)分别装有属于工业上“三酸两碱”中的“三种浓酸”和“两碱固体”.
(1)小袁同学没有利用任何试剂就鉴定出了C、D、E三瓶中的三种浓酸.他的做法是:①直接观察试剂瓶颜色,棕色试剂瓶E内的是______(填名称);②分别打开C、D瓶的瓶塞,观察到______,说明C瓶内的是浓盐酸,D瓶内的是浓硫酸.
(2)小白同学在查阅A、B瓶内的“两碱”的制备方法时,根据收集的信息,绘制了如下一个框图.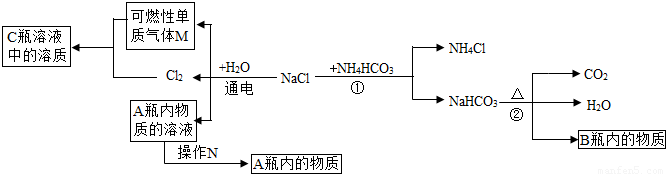
注:整个框图中每个化学反应涉及的物质已全部给出.
根据框图,依据化学反应前后元素种类守恒的相关知识,回答下列问题.
Ⅰ.写出下列物质化学式:A瓶内的物质:______.小袁同学认为工业生产中原料不能完全转化为产品,所以A瓶内的物质中一定含有杂质.请你帮助他设计出检验该杂质的实验方案(写出操作、现象和结论):______.
Ⅱ.框图中的①反应所属的反应类型是______. 请根据下表写出①反应能够发生的理由:______
NaCl、NH4HCO3、NaHCO3、NH4Cl在30℃时的溶解度如下表所示:
.请选用一种物理方法鉴别A、B瓶内的物质:______.
(3)小顾同学想利用D瓶内溶质质量分数为98%的浓硫酸来配制10%的稀硫酸196g,配制时应注意______.

(1)小袁同学没有利用任何试剂就鉴定出了C、D、E三瓶中的三种浓酸.他的做法是:①直接观察试剂瓶颜色,棕色试剂瓶E内的是______(填名称);②分别打开C、D瓶的瓶塞,观察到______,说明C瓶内的是浓盐酸,D瓶内的是浓硫酸.
(2)小白同学在查阅A、B瓶内的“两碱”的制备方法时,根据收集的信息,绘制了如下一个框图.

注:整个框图中每个化学反应涉及的物质已全部给出.
根据框图,依据化学反应前后元素种类守恒的相关知识,回答下列问题.
Ⅰ.写出下列物质化学式:A瓶内的物质:______.小袁同学认为工业生产中原料不能完全转化为产品,所以A瓶内的物质中一定含有杂质.请你帮助他设计出检验该杂质的实验方案(写出操作、现象和结论):______.
Ⅱ.框图中的①反应所属的反应类型是______. 请根据下表写出①反应能够发生的理由:______
NaCl、NH4HCO3、NaHCO3、NH4Cl在30℃时的溶解度如下表所示:
| 温度 | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30℃ | 41.1g | 27.0g | 11.1g | 36.3g |
(3)小顾同学想利用D瓶内溶质质量分数为98%的浓硫酸来配制10%的稀硫酸196g,配制时应注意______.