题目内容
氢化钙(CaH2)固体是登山队员常用的能源提供剂,用它与水反应生成氢氧化钙和氢气,氢气供燃烧之需.现有84g氢化钙与足量水反应,可生成多少克H2?在标况下,这些H2的体积是多少?(H2的密度在标况下为0.09g/L)
【答案】分析:根据氢化钙与足量水反应的化学方程式和氢化钙的质量,列出比例式,即可计算出生成H2质量;然后根据“体积=质量÷密度”即可计算出这些H2的体积.
解答:解:设生成H2质量为x
CaH2+2H2O═Ca(OH)2+2H2↑
42 4
84g x
∴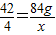
解得:x=8g,
这些H2的体积V=8g÷0.09g/L=88.9L.
答:生成H2质量为8g;这些H2的体积为88.9L.
点评:本题主要考查学生运用化学方程式进行计算的能力;学生需认真分析数量关系,认真计算,才能正确解答.
解答:解:设生成H2质量为x
CaH2+2H2O═Ca(OH)2+2H2↑
42 4
84g x
∴
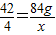
解得:x=8g,
这些H2的体积V=8g÷0.09g/L=88.9L.
答:生成H2质量为8g;这些H2的体积为88.9L.
点评:本题主要考查学生运用化学方程式进行计算的能力;学生需认真分析数量关系,认真计算,才能正确解答.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目

