题目内容
16.用侯氏制碱法制得的纯碱中含有一定量的氯化钠.现称取只含氯化钠的纯碱样品34.6g放入盛有130g稀盐酸的烧杯中,恰好完全反应,反应后溶液的质量为151.4g.请计算:样品中碳酸钠的质量.【C:12 O:16 Na:23】分析 解题的关键是能分析出溶液减少的原因是生成的二氧化碳跑掉了,可通过质量守恒定律求出生成的二氧化碳的质量,然后以二氧化碳的质量作为已知条件结合化学方程式进行计算.
解答 解:二氧化碳的质量为:130g+34.6g-151.4g=13.2g;
设样品中碳酸钠的质量为x,生成氯化钠的质量为y,稀盐酸中溶质的质量为z.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 13.2 g
$\frac{106}{44}=\frac{x}{13.2g}$
x=31.8g
答:样品中碳酸钠的质量为31.8g.
点评 本题主要考查学生运用化学方程式和质量守恒定律进行计算的能力.

练习册系列答案
相关题目
6.下列物质发生的变化属于化学变化的是( )
| A. | 加热石油分馏出来汽油和柴油等 | B. | 分离液态空气制取氧气 | ||
| C. | 过滤除去粗盐中含有的泥沙 | D. | 钢铁中潮湿空气中生锈 |
7.下列化学实验中都利用了水,不能体现水的主要作用的是( )
| A. |  防止熔融物落下使集气瓶底炸裂 | |
| B. |  吸收二氧化硫以防污染空气 | |
| C. |  排出集气瓶中的空气,便于收集到纯净的气体 | |
| D. |  提供热量,使白磷温度达到着火点 |
4.下列对于质量守恒定律的认识错误的是( )
| A. | 研究的是化学变化前后物质总质量的变化而不是研究物理变化中物质质量的变化 | |
| B. | 从宏观上看:化学反应中参与反应的所有反应物的总质量等于所有生成物总质量 | |
| C. | 从微观上看:化学反应前后原子的种类、原子数目、原子质量都保持不变 | |
| D. | 化学反应前后元素的质量可能会增大 |
1.下列物质按照单质、化合物、混合物顺序排列的是( )
| A. | 石墨 澄清石灰水 天然气 | B. | 黄铜 碳酸 石灰石 | ||
| C. | C60 碳酸钙 稀盐酸 | D. | 金刚石 二氧化碳 纯碱 |
8.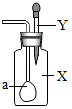 某化学兴趣小组同学利用下列各组物质做了一个有趣的化学实验如图:导管中吸有某种液体Y,广口瓶内盛有某种固体或者气体X;挤下导管内物质Y后,观察到气球a逐渐胀大.则不会产生上述现象的一种物质是( )
某化学兴趣小组同学利用下列各组物质做了一个有趣的化学实验如图:导管中吸有某种液体Y,广口瓶内盛有某种固体或者气体X;挤下导管内物质Y后,观察到气球a逐渐胀大.则不会产生上述现象的一种物质是( )
 某化学兴趣小组同学利用下列各组物质做了一个有趣的化学实验如图:导管中吸有某种液体Y,广口瓶内盛有某种固体或者气体X;挤下导管内物质Y后,观察到气球a逐渐胀大.则不会产生上述现象的一种物质是( )
某化学兴趣小组同学利用下列各组物质做了一个有趣的化学实验如图:导管中吸有某种液体Y,广口瓶内盛有某种固体或者气体X;挤下导管内物质Y后,观察到气球a逐渐胀大.则不会产生上述现象的一种物质是( )| A | B | C | D | |
| X | 硝酸铵固体 | 二氧化碳气体 | 氨气 | 生石灰固体 |
| Y | 蒸馏水 | NaOH溶液 | 稀盐酸 | 蒸馏水 |
| A. | A | B. | B | C. | C | D. | D |
14.2002年5月31是第15个世界无烟日,其主题是“无烟体育,清洁的比赛”,本届世界杯足球赛也因此定于2002年5月31日开幕.香烟燃烧产生的烟雾中含有尼古丁、煤焦油、一氧化碳等许多种有毒物质.你认为下列说法正确的是( )
| A. | 有毒气体均为气味 | |
| B. | 香烟烟雾是一种纯净物 | |
| C. | 尼古丁[C10H14N2]中,碳、氢、氮三种元素的质量比是10:14:2 | |
| D. | 一氧化碳能和血液里的血红蛋白结合而引起中毒 |