题目内容
根据下图所示的实验装置,回答以下问题:

(1)图中标有①、②的仪器名称:①________;②________.
(2)A装置中试管口略向下倾斜的目的是________________.
(3)在加入药品之前应对实验装置进行________________.
(4)可用于实验室制备和收集O2的一套装置是(填序号)________.
(5)写出用石灰石和稀盐酸制取二氧化碳可选用图中________和________(填序号)组装一套制取二氧化碳的装置.检验二氧化碳集满的方法是________________.
(6)乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔.你认为制取乙炔应选择的发生装置是________;收集装置是________.
解析:
|
答案:(1)长颈漏斗 集气瓶 (2)防止冷凝水倒流而引起试管破裂 (3)装置的气密性检查 (4)AC(或AD、BC、BD均可) (5)B C 用燃着的木条放在集气瓶口,观察燃着木条是否熄灭 (6)B D 讲析:(1)图中标有①、②的仪器名称分别是长颈漏斗、集气瓶.(2)A装置中试管口略向下倾斜的目的是防止冷凝水倒流而导致试管破裂.(3)在实验室制取气体的实验中,加入药品前要检查装置的气密性.(4)若采用加热高锰酸钾的方法制取氧气,因反应物是固体,且需要加热,故需用“固-固加热装置”,即A.氧气不易溶于水,且密度比空气略大,可选用C或D装置收集;若采用分解过氧化氢溶液的方法制取氧气,因为反应物是液体,且不需要加热,故需用“固(指催化剂二氧化锰)-液不加热装置”,即B.收集装置仍是C或D.(5)实验室制取二氧化碳的反应物是石灰石和稀盐酸,反应不需加热,生成的二氧化碳气体能溶于水,故应选择B和C的组合来作制取装置;检验二氧化碳气体是否收集满的方法是将燃着的火柴放在集气瓶口,若火柴熄灭则证明气体已经收集满.(6)根据“用电石(固体)与水反应制取乙炔”,可推知其发生装置为B,再根据“密度比空气略小,不溶于水”,可推知其收集装置需用D,因乙炔的密度只是略小于空气,故不宜采用向下排空气法收集. 点评:实验室制取氧气是教材多年保留的经典实验,在中考中考查频度极高.考查热点有:识别所用化学仪器的名称、了解其主要用途及使用时的注意事项;会依据反应原理确定气体发生装置,会依据气体的性质确定收集装置;掌握实验原理、步骤及注意事项等;能将由制氧气提炼出的原理顺利地迁移到其他气体(如,二氧化碳、氢气等)以及未知气体的制取中. |

小明同学从资料中得知,金属过氧化物常用作宇宙飞船或潜水艇中的氧气再生剂.对金属过氧化物用作氧气再生剂的化学原理,小明同学进行了如下探究,请你参与.
[查阅资料]a.金属过氧化物(如过氧化钠:Na2O2)能与二氧化碳反应生成一种白色固体和氧气;
b.过氧化钠与水、盐酸等物质反应也能生成氧气;
c.碳酸氢钠能与盐酸反应生成碳酸钠、水和二氧化碳,而碳酸氢钠与二氧化碳不反应.
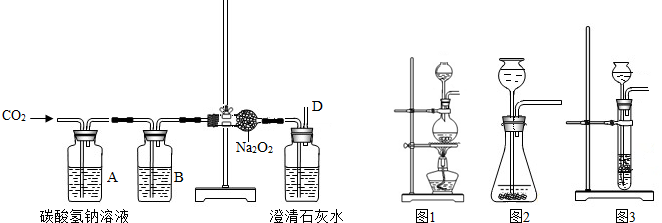
[设计实验]实验Ⅰ:小明同学用下图所示的实验验证反应生成了氧气.
(1)小明同学在实验室制取CO2时,选择发生装置时应考虑的因素是______(填序号).
A.反应物的状态B.CO2的溶解度和密度
C.反应是否需要加热D.CO2是否有毒
(2)根据上述因素,制取CO2时,应从上图1、图2、图3中选择______.写出实验室制取二氧化碳的化学方程式______.
(3)设计A、B装置的目的是得到纯净且干燥的CO2气体.其中A装置的作用是______;B装置主要目的是干燥CO2气体,连接这一装置的理由是______,那么B中所装的试剂是______(填序号).
A.浓硫酸B.固体NaOH C.生石灰
(4)为了确定CO2根Na2O2反应产生的气体是氧气,最后还要采用的验证实验操作及现象是______.
(5)表明二氧化碳没有被过氧化钠完全吸收的现象是______,该反应的化学方程式为______.
实验Ⅱ探究反应生成的白色固体的成分.
[提出猜想]①该白色固体是氢氧化钠;②该白色固体是碳酸钠.
小明的两个猜想中一定错误的是猜想______(选填“①”或“②”),理由是______.
[设计实验]小明通过以下实验验证了另一个猜想是正确的.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量反应后的固体于试管中; ②_____________; ③_____________. | ②_________; ③_________. | 猜想_________(选填“①”或“②”)正确. |
(2)请你根据上述实验简述过氧化钠作为氧气再生剂的化学反应原理______.
[查阅资料]a.金属过氧化物(如过氧化钠:Na2O2)能与二氧化碳反应生成一种白色固体和氧气;
b.过氧化钠与水、盐酸等物质反应也能生成氧气;
c.碳酸氢钠能与盐酸反应生成碳酸钠、水和二氧化碳,而碳酸氢钠与二氧化碳不反应.
[设计实验]实验Ⅰ:小明同学用下图所示的实验验证反应生成了氧气.

(1)小明同学在实验室制取CO2时,选择发生装置时应考虑的因素是______(填序号).
A.反应物的状态B.CO2的溶解度和密度
C.反应是否需要加热D.CO2是否有毒
(2)根据上述因素,制取CO2时,应从上图1、图2、图3中选择______.写出实验室制取二氧化碳的化学方程式______.
(3)设计A、B装置的目的是得到纯净且干燥的CO2气体.其中A装置的作用是______;B装置主要目的是干燥CO2气体,连接这一装置的理由是______,那么B中所装的试剂是______(填序号).
A.浓硫酸B.固体NaOH C.生石灰
(4)为了确定CO2根Na2O2反应产生的气体是氧气,最后还要采用的验证实验操作及现象是______.
(5)表明二氧化碳没有被过氧化钠完全吸收的现象是______,该反应的化学方程式为______.
实验Ⅱ探究反应生成的白色固体的成分.
[提出猜想]①该白色固体是氢氧化钠;②该白色固体是碳酸钠.
小明的两个猜想中一定错误的是猜想______(选填“①”或“②”),理由是______.
[设计实验]小明通过以下实验验证了另一个猜想是正确的.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量反应后的固体于试管中; ②_____________; ③_____________. | ②_________; ③_________. | 猜想_________(选填“①”或“②”)正确. |
(2)请你根据上述实验简述过氧化钠作为氧气再生剂的化学反应原理______.