题目内容
1.地质考察人员发现一种带螺纹的矿石,研究时发现该矿石能在氧气中燃烧,主要反应是:4X+11O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+8SO2.下列有关说法中不正确的是( )| A. | X的化学式是FeS2 | B. | SO2中硫元素的化合价是+4 | ||
| C. | 该反应是复分解反应 | D. | Fe2O3中铁元素的质量分数为70% |
分析 A、化学反应前后,元素的种类不变,原子的种类、总个数不变;
B、根据化合价的原则,进行分析;
C、根据化学方程式的反应物、生成物种类,判定反应类型;
D、关键物质的化学式可以计算组成元素的质量分数.
解答 解:A、由4X+11O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+8SO2可知,每个X中含有1个铁原子和2个硫原子,是二硫化亚铁,化学式是FeS2,该选项说法正确;
B、根据化合价的原则:化合物中,元素的化合价代数和为零,结合氧元素的化合价为-2价,则SO2中硫元素的化合价是+4,该选项说法正确;
C、根据4X+11O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+8SO2可知,该反应不是分解反应,该选项说法不正确;
D、Fe2O3中铁元素的质量分数为:$\frac{56×2}{56×2+16×3}$×100%=70%,该选项说法正确.
故选:C.
点评 需要考虑:单质中,因为没有元素之间的化合,所以规定单质中元素的化合价为零;化合物中,元素的化合价代数和为零,这是判断物质的化学式或元素化合价是否正确的依据.

练习册系列答案
相关题目
11.初中化学学业水平考试实行网上阅卷,考生答题时必须使用2B铅笔填涂答题卡,2B铅笔芯的主要成分是
( )
( )
| A. | 石墨 | B. | 木炭 | C. | 焦炭 | D. | 铅 |
12.下列物质属于纯净物的是( )
| A. | 豆浆 | B. | 空气 | C. | 酒精 | D. | 酱油 |
9.下列有关实验的现象描述正确的是( )
| A. | 一氧化碳通入澄清石灰水中,澄清石灰水变浑浊 | |
| B. | 打开浓盐酸的瓶塞时,瓶口冒白雾 | |
| C. | 点燃棉纱线和羊毛线,都有烧焦羽毛的气味 | |
| D. | 在空气中点燃镁条,发出耀眼的强光,生成黑色固体 |
6.下列物质的用途中,错误的是( )
| A. | 碳酸钙用作补钙剂 | B. | 干冰用于人工降雨 | ||
| C. | 氢氧化钠用于改良酸性土壤 | D. | 浓硫酸用作气体干燥剂 |
13.如图是某反应的微观示意图,下列说法不正确的是( )
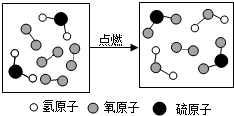

| A. | 反应物中有单质 | B. | 该反应为置换反应 | ||
| C. | 生成物的分子个数比为1:1 | D. | 化学反应前后原子的种类不变 |
10.根据如表提供的信息,下列判断正确的是( )


| A. | 元素所在的周期数等于其原子的核外电子数 | |
| B. | 钠离子核外有三个电子层 | |
| C. | 第二、三周期元素的原子从左至右最外层电子数逐渐增多 | |
| D. | 在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg2+ |