题目内容
小科同学为测定某铁合金的含铁量,做了如下实验,称取11.4g样品,放入质量为50g的烧杯中,再往烧杯内加入足量的100.0g稀盐酸(杂质不与酸反应,不溶于水),并对烧杯进行了四次称量,记录的数据如下:
| 反应时间 | t1 | t2 | t3 | t4 |
| 烧杯总质量/g | 161.4 | 161.2 | 161.0 | 161.0 |
(1)反应中产生的氢气质量是多少?
(2)稀盐酸中溶质的质量分数是多少?
(3)应后溶液中氯化亚铁的质量分数(本题计算结果准确到0.1%).
解:(1)分析题干给出的数据以及表格的数据可知此反应进行完全,根据质量守恒定律,可得产生氢气的质量为:
11.4g+100.0g+50g-161.0g=0.4g;
(2)设产生0.4g氢气同时生成氯化亚铁的质量为x,需要氯化氢的质量为y,则有
Fe+2HCl=FeCl2+H2↑
73 127 2
y x 0.4g
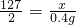
x=25.4g
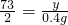
y=14.6g
稀盐酸中溶质的质量分数=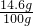 ×100%=14.6%.
×100%=14.6%.
(3)反应后溶液中氯化亚铁的质量分数=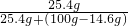 ×100%≈22.9%
×100%≈22.9%
答:(1)反应产生的氢气的质量为0.4g;
(2)稀盐酸中溶质的质量分数为14.6%;
(3)反应后溶液中氯化亚铁的质量分数为22.9%.
分析:测定某铁合金的含铁量,实际上就是利用金属铁与酸反应生成氢气的质量进行的计算,要分析表格中给出的数据,得出正确的结论.
点评:此题考查的是混合物中纯物质的含量的计算,完成此类题目,要分析题干中涉及到的化学反应,根据质量守恒定律计算出某物质的质量,然后进行计算.
11.4g+100.0g+50g-161.0g=0.4g;
(2)设产生0.4g氢气同时生成氯化亚铁的质量为x,需要氯化氢的质量为y,则有
Fe+2HCl=FeCl2+H2↑
73 127 2
y x 0.4g
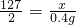
x=25.4g
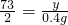
y=14.6g
稀盐酸中溶质的质量分数=
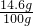 ×100%=14.6%.
×100%=14.6%.(3)反应后溶液中氯化亚铁的质量分数=
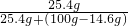 ×100%≈22.9%
×100%≈22.9%答:(1)反应产生的氢气的质量为0.4g;
(2)稀盐酸中溶质的质量分数为14.6%;
(3)反应后溶液中氯化亚铁的质量分数为22.9%.
分析:测定某铁合金的含铁量,实际上就是利用金属铁与酸反应生成氢气的质量进行的计算,要分析表格中给出的数据,得出正确的结论.
点评:此题考查的是混合物中纯物质的含量的计算,完成此类题目,要分析题干中涉及到的化学反应,根据质量守恒定律计算出某物质的质量,然后进行计算.

练习册系列答案
相关题目
小可同学为测定某铁合金的含铁量,做了如下实验,称取11.4克样品,放入质量为50.0克的烧杯中,再往烧杯中加入100.0克的稀盐酸(杂质不与酸反应、不溶于水)并对烧杯进行了四次称量,记录数据如下:
求:(1)反应产生的氢气的质量
(2)该铁合金中铁的质量分数(保留一位小数)
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯总质量/g | 161.4 | 161.2 | 161.0 | 161.0 |
(2)该铁合金中铁的质量分数(保留一位小数)
小科同学为测定某铁合金的含铁量,做了如下实验,称取11.4g样品,放入质量为50g的烧杯中,再往烧杯内加入足量的100.0g稀盐酸(杂质不与酸反应,不溶于水),并对烧杯进行了四次称量,记录的数据如下:
求:
(1)反应中产生的氢气质量是多少?
(2)稀盐酸中溶质的质量分数是多少?
(3)应后溶液中氯化亚铁的质量分数(本题计算结果准确到0.1%).
| 反应时间 | t1 | t2 | t3 | t4 |
| 烧杯总质量/g | 161.4 | 161.2 | 161.0 | 161.0 |
(1)反应中产生的氢气质量是多少?
(2)稀盐酸中溶质的质量分数是多少?
(3)应后溶液中氯化亚铁的质量分数(本题计算结果准确到0.1%).