题目内容
在中学的化学实验中,实验室经常用锌与稀硫酸制取氢气.
(1)写出实验室制取氢气的化学方程式______.
(2)若用该方法制得氢气为0.4g,则反应中消耗的锌的质量为______ g,若同时消耗了100g稀硫酸溶液,则稀硫酸溶液中溶质的质量分数为______%
解:(1)反应物是锌和硫酸,生成物是硫酸锌和氢气,氢气后面标上上升符号,所以方程式是:Zn+H2SO4=ZnSO4+H2↑;
(2)设制得0.4g氢气,反应需要锌的质量为x,消耗硫酸的质量为y则:
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y 0.4g
根据: 解得x=13g,根据:
解得x=13g,根据: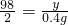 解得y=19.6g,所以稀硫酸溶液中溶质的质量分数为:
解得y=19.6g,所以稀硫酸溶液中溶质的质量分数为: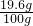 ×100%=19.6%.
×100%=19.6%.
故答案为:(1)Zn+H2SO4=ZnSO4+H2↑;(2)13;19.6.
分析:首先正确写出锌和稀硫酸反应的化学方程式,然后根据方程式,利用氢气的质量求出需要金属锌的质量和消耗的硫酸的质量,用硫酸的质量除以100g乘以百分之百即可.
点评:此题是根据化学方程式的计算题,该题比较简单,就是用一种生成物的质量求一种反应物的质量,属于最基本类型的计算题.
(2)设制得0.4g氢气,反应需要锌的质量为x,消耗硫酸的质量为y则:
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y 0.4g
根据:
 解得x=13g,根据:
解得x=13g,根据: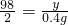 解得y=19.6g,所以稀硫酸溶液中溶质的质量分数为:
解得y=19.6g,所以稀硫酸溶液中溶质的质量分数为: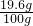 ×100%=19.6%.
×100%=19.6%.故答案为:(1)Zn+H2SO4=ZnSO4+H2↑;(2)13;19.6.
分析:首先正确写出锌和稀硫酸反应的化学方程式,然后根据方程式,利用氢气的质量求出需要金属锌的质量和消耗的硫酸的质量,用硫酸的质量除以100g乘以百分之百即可.
点评:此题是根据化学方程式的计算题,该题比较简单,就是用一种生成物的质量求一种反应物的质量,属于最基本类型的计算题.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目

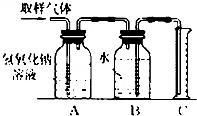 13、据2000年12月18日《厦门日报》“学校化学实验室也是污染源”一文指出:全国数以万计的高校、中学的化学实验室每天都排放着成分复杂的污染物.为此某学校化学研究小组拟进行如下实验,以粗略测试刚做完实验的实验室(甲)空气中全部酸性气体的含量.
13、据2000年12月18日《厦门日报》“学校化学实验室也是污染源”一文指出:全国数以万计的高校、中学的化学实验室每天都排放着成分复杂的污染物.为此某学校化学研究小组拟进行如下实验,以粗略测试刚做完实验的实验室(甲)空气中全部酸性气体的含量.