题目内容
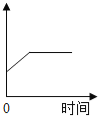
【题目】下图是以空气等为原料合成尿素![]() 的流程(部分产物略去)。
的流程(部分产物略去)。

请按要求回答相关问题:
(1)Y气体在空气中的体积分数为![]() ,它的化学式是__________
,它的化学式是__________
(2)分离空气的主要方法是将液态空气气化,首先从液态空气中蒸发出来的是__________,此过程发生的是__________变化。
(3)反应①的基本类型是__________。
(4)反应②生成尿素的同时还生成相对分子质量最小的氧化物,写出反应②的符号表达式__________。
【答案】CO2 氮气 物理 化合反应 H2O
【解析】
(1)Y气体在空气中的体积分数为![]() ,Y是CO2。
,Y是CO2。
(2)液氮的沸点低,分离空气的主要方法是将液态空气气化,首先从液态空气中蒸发出来的是氮气,此过程中无新物质生成,发生的是物理变化。
(3)反应①是碳与氧气反应生成二氧化碳,由两种或两种以上的物质发生化学反应生成另一种物质的反应是化合反应,该反应的基本类型是化合反应。
(4)相对分子质量最小的氧化物是H2O。

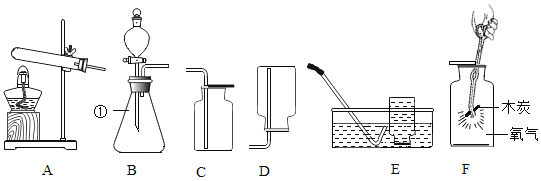
【题目】同学们在研究氧气性质时,进行了如图1的实验;取一段打磨好的螺旋状铁丝,在下端系一根火柴,点燃火柴,待火柴快燃尽时,插入充满氧气且放有少量水的集气瓶中,观察到如下现象:
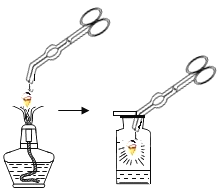
银白色的铁丝在氧气中剧烈燃烧,________,放出大量的热,生成黑色固体物质。该实验说明铁丝能够在氧气中燃烧,氧气具有助燃性。
小明在阅读相关资料时发现二氧化氮也具有助燃性,他决定利用如下实验进行探究。
(提出问题)二氧化氮是否具有助燃性?
(查阅资料)
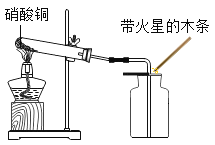
①蓝色的硝酸铜固体在加热条件下分解生成氧化铜、二氧化氮和氧气。
②氧化铜是一种黑色固体,通常状况下,二氧化氮是一种红棕色气体,相同状况下,其密度大于氧气密度,在低于室温时变成液态。
(实验过程)
实验装置 | 实验现象 | 实验结论 |
| 试管内蓝色固体逐渐变为黑色,有红棕色气体生成,________。 | 二氧化氮具有助燃性。 |
(反思与评价)
小刚认为小明的实验不能证明![]() 具有助燃性,其理由是________.
具有助燃性,其理由是________.
小刚认为利用补充如下实验可以证明![]() 具有助燃性.
具有助燃性.
实验操作 | 实验现象 | 实验结论 |
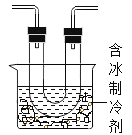
步骤I:在上图的试管和集气瓶之间连上如图所示的装置,重新进行加热硝酸铜的实验
| 带火星的木条复燃。 | 硝酸铜分解产物中有________。 |
步骤II:取出图中的U型管,恢复至室温,待U型管内充满红棕色气体时,将带火星的木条伸入U型管中。 | 带火星的木条复燃。 |
|
小红认为即使不进行小刚的实验,依据资料和小明的实验现象也能推出![]() 具有助燃性,其理由是________。
具有助燃性,其理由是________。
【题目】空气是宝贵的自然资源。利用氢气(H2)和空气中分离出的氮气(N2)可以合成氨气(NH3),下列是合成氨的工艺流程图:

(1)工业上用分离液态空气的方法获得氮气。将空气液化后再气化,首先分离出氮气,剩下的主要是液氧。
根据下表中各物质的沸点,如要将产物 NH3与 N2、H2分离开来,温度应该控制在______℃的范围之内。
物质 | H2 | N2 | NH3 |
沸点/℃ | -252 | -195.8 | -33.4 |
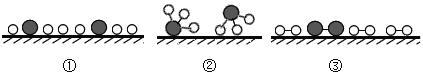
(2)用“〇”表示氢原子,“![]() ”表示氮原子,“
”表示氮原子,“![]() ”表示催化剂,观察下列微观图,合成氨化学反应过程的微观顺序为________(将下面三张图用序号排列)。
”表示催化剂,观察下列微观图,合成氨化学反应过程的微观顺序为________(将下面三张图用序号排列)。
(3)用焦炭(主要成分是碳)和水蒸气在高温条件下反应可制得氢气和另一种常温下为气态的有毒物质,写出该反应的文字表达式_____________。在煤和水蒸气反应前需先将煤粉碎,这样做的目的是_____________。
(4)实际生产中,N2和H2不可能全部转化为NH3。将降温分离出的N2、H2送回合成塔的目的是______。
A充分利用原料 B防止氮气污染空气
【题目】(7分)化学是在原子、分子水平上研究物质及其变化的科学。
(1)现有下列化学式或微粒符号:①2CO、②Ca2+、③2H、④O2。其中,“2”表示2个分子的是 (填序号,下同),表示每个微粒带2个单位电荷的是_______。
(2)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如下。下列说法正确的是 (填选项)。
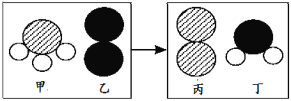
A 反应前后共有4种原子 B 该反应有单质生成
C 反应前后元素化合价都不变 D 化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2∶3
(3)胃酸过多须服用抗酸药。下表为两种抗酸药的有效成分及其构成微粒:
抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
构成微粒 | Mg2+、OH— | Al3+、Mg2+、OH-、CO32- |
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异。
①Mg(OH)2起抗酸作用的微粒是 (填微粒符号,下同)。
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl=MgCl2+AlCl3+4H2O+CO2↑。则
铝碳酸镁起抗酸作用的两种微粒是 、 。