题目内容
7.甲、乙两同学想了解碳酸钠溶液的酸碱性.他们做了以下研究:| 实 验 操 作 | 检测结果 | |
| 甲同学 | 取pH试纸放在玻璃片上; 用玻璃棒蘸取碳酸钠溶液沾在pH试纸上; 将试纸显示的颜色与标准比色卡比较. | pH>7 |
| 乙同学 | 将pH试纸直接浸入碳酸钠溶液中,把试纸显示的颜色与标准比色卡比较. | PH>7 |
(2)请帮甲同学将步骤补充完整.根据两位同学的实验操作,你认为乙同学操作不规范.为什么?污染试剂
(3)如果实验室没有pH试纸,又要一次测定未知溶液的酸碱性,可选用紫色石蕊试液来进行实验,该试剂从紫色变成蓝色,能确定其酸碱性.用盐酸可以将铝壶内壁上的水垢[主要成分是Mg(OH)2和CaCO3]除去,原理是(用化学方程式表示)CaCO3+2HCl═CaCl2+H2O+CO2↑、Mg(OH)2+2HCl═MgCl2+2H2O
但所用盐酸不能过量,否则,铝壶将被腐蚀,其原因是(用化学方程式表示)2Al+6HCl═2AlCl3+3H2↑.
分析 (1)根据pH>7的溶液显碱性解答;
(2)根据使用pH试纸测定溶液酸碱度的正确方法是:将pH试纸放在玻璃片上,用玻璃棒蘸取被测液沾到pH试纸上,将试纸显示的颜色与标准比色卡比较,得出溶液的pH.不能把pH试纸放入被测液中,这样会污染试剂;
(3)要测定溶液的酸碱性,还可以使用酸碱指示剂,例如紫色石蕊溶液遇酸会变红,遇碱性溶液会变蓝;根据盐酸能够和碳酸钙、氢氧化镁、铝等反应产生反应的方程式.
解答 解:使用pH试纸测定溶液酸碱度的正确方法是:将pH试纸放在玻璃片上,用玻璃棒蘸取被测液沾到pH试纸上,将试纸显示的颜色与标准比色卡比较,得出溶液的pH;故答案为:玻璃片;玻璃棒;
(1)由甲同学的实验可知溶液的pH>7,所以溶液显碱性;故答案为:碳酸钠溶液显碱性;
(2)使用pH试纸测定溶液酸碱度时,不能把pH试纸直接放入被测液中,这样会污染试剂;故答案为:乙;污染试剂;
(3)使用酸碱指示剂可以测定溶液的酸碱性,例如紫色石蕊溶液遇酸会变红,遇碱性溶液会变蓝,无色酚酞溶液遇酸不变色,遇碱溶液变红色;
水垢的主要成分碳酸钙和氢氧化镁难溶于水,能与酸反应,可用稀盐酸除去.碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.氢氧化镁和盐酸反应生成氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl═MgCl2+2H2O;当水垢完全反应后,铝稀盐酸发生反应,生成氯化铝与氢气,故不能长时间浸泡,反应的化学方程式为:2Al+6HCl═2AlCl3+3H2↑;
故答案为:紫色石蕊;紫;蓝;CaCO3+2HCl═CaCl2+H2O+CO2↑;Mg(OH)2+2HCl═MgCl2+2H2O;2Al+6HCl═2AlCl3+3H2↑;
点评 本题主要考查测定溶液酸碱度和酸碱性的正确方法及根据反应原理书写化学方程式的能力,要求我们严格按照正确操作方法进行实验并熟练正确的书写反应的方程式,难度不大.

| A. | 氧气是一种无色无味的气体 | B. | 铝能在一定条件下被氧气氧化 | ||
| C. | 氢气具有还原性 | D. | 碳酸能使紫色石蕊试液变成红色 |
| A. | 稀盐酸 | B. | 二氧化碳气体 | C. | 石蕊试液 | D. | 酚酞试液 |
| A. | 地球上水的总量多,淡水少 | |
| B. | “南水北调”工程说明南方水的储量多,北方水的储量少 | |
| C. | 我国水资源总量多,人均水量少 | |
| D. | 生活中接触的纯净水多,水溶液少 |
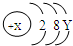
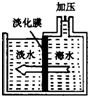 海洋中蕴含丰富的资源.
海洋中蕴含丰富的资源.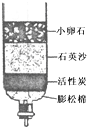 水是生命之源,也是人类最宝贵的资源.试用你学过的化学知识,回答下列问题:
水是生命之源,也是人类最宝贵的资源.试用你学过的化学知识,回答下列问题: