题目内容
现有四种物质 ① NaOH ② H2SO4 ③ MgCl2、 ④ SO3,
(1)其中属于盐的是__________________(填序号),属于氧化物的是_________(填序号)
(2)在一定条件下,能相互反应生成盐和水,且不属于中和反应的化学方程式为_____________。
③, ④。 SO3+2NaOH=Na2SO4+H2O 【解析】(1)由金属或铵根和酸根组成的化合物叫盐,由两种元素组成,且其中一种是氧的化合物叫氧化物。其中属于盐的是MgCl2,属于氧化物的是SO3;(2)非金属氧化物和碱在一定条件下,能相互反应生成盐和水,且不属于中和反应,化学方程式为SO3+2NaOH=Na2SO4+H2O。 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案下列实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向醋酸中加入氢氧化钠溶液 | 无明显现象 | 二者之间不发生反应 |
B | 向溶质质量分数为5%的过氧化氢溶液中加入少量氧化铜 | 有大量气泡产生 | 氧化铜起催化作用 |
C | 将两根铁丝分别伸入硫酸铜溶液和硝酸银溶液中 | 两根铁丝上均有固体附着 | 金属的活动性顺序为 Fe>Cu>Ag |
D | 用导管分别对准浸没在热水和冷水中的白磷通气 | 热水中的白磷燃烧,冷水中的白磷不燃烧 | .燃烧的条件之一是温度达到着火点 |
A. A B. B C. C D. D
D 【解析】A、向醋酸中加入氢氧化钠溶液,二者之间发生中和反应,但反应无明显现象,常需要借助于酸碱指示剂判断反应的发生,错误; B、催化剂的作用叫催化作用。催化剂就是能改变其它物质的反应速率,而本身的质量和化学性质在反应前后不变的物质。向溶质质量分数为5%的过氧化氢溶液中加入少量氧化铜,有大量气泡产生,但没有证明反应前后氧化铜的质量和化学性质不变,不能确定是催化剂,错误;C 、在金属活动性顺...为了探究石灰石的纯度(假设样品中的杂质既不溶于水也不与盐酸反应),称取80g石灰石样品等分为4份(分别编号为①、②、③、④),每份样品分别与一定量的稀盐酸反应,所得数据如表所示:
样品编号 | ① | ② | ③ | ④ |
稀盐酸的质量 | 50g | 100g | m(150<m<250) | 250g |
剩余固体的质量 | 15g | 10g | 4g | 4g |
然后,为了探究石灰石与稀盐酸反应后所得溶液中的溶质成分,将编号③所得溶液过滤,取滤液质量的1/8于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示:
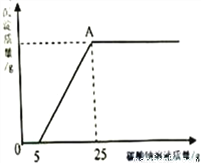
分析题中有关信息和图表(横坐标表示碳酸钠溶液、纵坐标为生成沉淀质量),回答下列问题:
(1)该石灰石样品的纯度为______.所用盐酸的溶质质量分数为__________。
(2)编号③所用稀盐酸的质量m为______g.
(3)A点处对应的溶液中溶质的质量是________?(写出计算过程)
80% 7.3% 200克 29.25克 【解析】【解析】 (1)该石灰石样品的纯度为×100%=80%; 50g盐酸消耗的碳酸钙质量为20g-15g=5g,设50g盐酸的溶质质量为x CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 73 5g x x=3.65g 所用盐酸的溶质质量分数为×100%=7.3%; (2)设编号③...



