题目内容
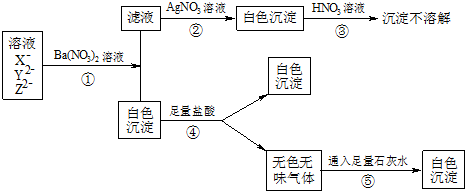
某溶液中含有X-、Y2-、Z2-三种常见的无机离子.如下图框图所示,发生了一系列化学反应.
(1)判断X-、Y2-、Z2-分别为
(2)写出①、②、④、⑤步反应的离子方程式.
①

(1)判断X-、Y2-、Z2-分别为
Cl-、
Cl-、
、CO32-或SO42-
CO32-或SO42-
、SO42-或CO32-
SO42-或CO32-
(写离子符号).(2)写出①、②、④、⑤步反应的离子方程式.
①
SO42-+Ba2+=BaSO4↓;CO32-+Ba2+=BaCO3↓
SO42-+Ba2+=BaSO4↓;CO32-+Ba2+=BaCO3↓
②Cl-+Ag+=AgCl
Cl-+Ag+=AgCl
④2H++BaCO3=H2O+Ba2++CO2↑
2H++BaCO3=H2O+Ba2++CO2↑
⑤CO2+2OH-+Ca2+=CaCO3↓+H2O
CO2+2OH-+Ca2+=CaCO3↓+H2O
.分析:溶液中加入硝酸钡后产生白色沉淀,白色沉淀中加入盐酸沉淀部分溶解,说明沉淀中含有硫酸钡和碳酸钡,碳酸钡与盐酸反应能产生无色无味的气体二氧化碳,二氧化碳与石灰水反应能生成白色沉淀碳酸钙,故溶液中含有硫酸根离子和碳酸根离子;滤液中加入硝酸银产生不溶于硝酸的白色沉淀,说明溶液中含有氯离子,氯离子与银离子结合生成氯化银不溶于硝酸.据此分析解答.
解答:解:溶液中加入硝酸钡后产生白色沉淀,白色沉淀中加入盐酸沉淀部分溶解,说明沉淀中含有硫酸钡和碳酸钡,碳酸钡与盐酸反应能产生无色无味的气体二氧化碳,二氧化碳与石灰水反应能生成白色沉淀碳酸钙,故溶液中含有硫酸根离子和碳酸根离子;滤液中加入硝酸银产生不溶于硝酸的白色沉淀,说明溶液中含有氯离子,氯离子与银离子结合生成氯化银不溶于硝酸.
(1)由上述分析可知X-为氯离子,Y2-和Z2-为硫酸根离子和碳酸根离子,符号分别为 Cl-、SO42-、CO32-.
(2)①反应为硫酸根、碳酸根离子与钡离子结合成沉淀,离子方程式为SO42-+Ba2+=BaSO4↓;
CO32-+Ba2+=BaCO3↓
②反应为氯离子和银离子结合成氯化银,离子方程式为Cl-+Ag+=AgCl
④反应为盐酸中的氢离子与碳酸钡反应生成二氧化碳的过程,离子方程式为2 H++BaCO3=H2O+Ba2++CO2↑
⑤步反应为二氧化碳与石灰水反应,离子方程式CO2+2OH-+Ca2+=CaCO3↓+H2O.
故答案为:(1)Cl-、SO42- CO32-
(2)①SO42-+Ba2+=BaSO4↓;CO32-+Ba2+=BaCO3↓ ②Cl-+Ag+=AgCl
④2 H++BaCO3=H2O+Ba2++CO2↑ ⑤CO2+2OH-+Ca2+=CaCO3↓+H2O
(1)由上述分析可知X-为氯离子,Y2-和Z2-为硫酸根离子和碳酸根离子,符号分别为 Cl-、SO42-、CO32-.
(2)①反应为硫酸根、碳酸根离子与钡离子结合成沉淀,离子方程式为SO42-+Ba2+=BaSO4↓;
CO32-+Ba2+=BaCO3↓
②反应为氯离子和银离子结合成氯化银,离子方程式为Cl-+Ag+=AgCl
④反应为盐酸中的氢离子与碳酸钡反应生成二氧化碳的过程,离子方程式为2 H++BaCO3=H2O+Ba2++CO2↑
⑤步反应为二氧化碳与石灰水反应,离子方程式CO2+2OH-+Ca2+=CaCO3↓+H2O.
故答案为:(1)Cl-、SO42- CO32-
(2)①SO42-+Ba2+=BaSO4↓;CO32-+Ba2+=BaCO3↓ ②Cl-+Ag+=AgCl
④2 H++BaCO3=H2O+Ba2++CO2↑ ⑤CO2+2OH-+Ca2+=CaCO3↓+H2O
点评:熟练掌握离子的检验与鉴别是解答本题关键,并会写离子方程式

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



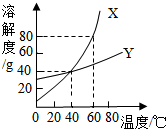 X、Y两种固体物质的溶解度曲线如图所示,某烧杯中含有X、Y两种物质在60℃时的饱和溶液,且烧杯底尚有少量的X、Y两种固体(若不考虑X、Y两种物质在同一溶液中的相互影响),随着温度的降低,则下列说法中正确的是( )
X、Y两种固体物质的溶解度曲线如图所示,某烧杯中含有X、Y两种物质在60℃时的饱和溶液,且烧杯底尚有少量的X、Y两种固体(若不考虑X、Y两种物质在同一溶液中的相互影响),随着温度的降低,则下列说法中正确的是( )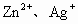 和
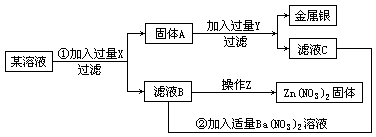
和 三种离子,为了从该溶液中提取金属银并得到硝酸锌,设计了以下实验步骤如图所示
三种离子,为了从该溶液中提取金属银并得到硝酸锌,设计了以下实验步骤如图所示