题目内容
用微粒的观点看世界是化学独特的视角,下列对宏观现象的微观解释错误的是( )
A. 食盐能溶解在水中,说明微粒是不断运动的
B. 流动的水变成固态的冰,是因为水分子自身能量降低而导致运动减慢
C. 20mL酒精和20mL水混合后体积小于40mL,是因为分子之间存在间隔
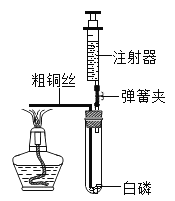
D. 在密闭的注射器内加热水,水变成水蒸气体积变大,是因为水分子体积变大了
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案区分下列各组物质,所加试剂或操作方法都正确的是( )
选项 | 需区分的物质 | 方法一 | 方法二 |
A | 烧碱和熟石灰 | 滴加稀盐酸,观察是否产生气泡 | 溶于水观察溶解性 |
B | 黄金和黄铜 | 灼烧后观察颜色 | 加入稀盐酸 |
C | 氧气和氢气 | 通入紫色石蕊试液 | 通过灼热的氧化铜 |
D | 食盐水和稀盐酸 | 闻气味 | 滴加硝酸银溶液 |
A.A B.B C.C D.D
Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
第1次 | 40 | m |
第2次 | 40 | 14.8 |
第3次 | 40 | 12.2 |
第4次 | 40 | 11.2 |
第5次 | 40 | 11.2 |
试回答下列问题:
(1)从以上数据可知,最后剩余的11.2g固体的成分是______;表格中,m=______。
(2)黄铜样品中锌的质量分数为______。
(3)计算所用稀硫酸中硫酸的质量分数是多少____?
(4)配制100g该浓度的稀硫酸需要质量分数为98%浓硫酸的质量是多少____?
下图是实验室制备气体的部分装置。
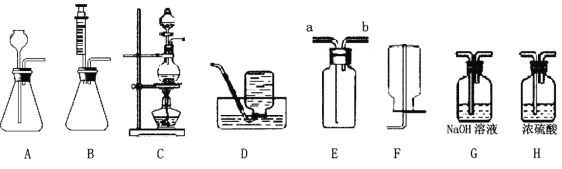
(1)上图装置可以制取不同气体,请完成下表空格。
反应物和反应条件 | 制取的气体 | 发生装置(填字母) | 收集装置(填字母) |
H2O2溶液和MnO2固体,常温 | ______ | A或B | 或E |
亚硫酸钠(Na2SO3)固体和浓硫酸,常温 | SO2 | ______ | E |
甲酸( HCOOH)和浓硫酸,加热 | CO | ______ | D |
(2)用A装置制取O2时,反应的化学方程式为____________________,若要得到干燥的O2,所选择装置的连接顺序为:A→____→ _____ (填字母序号)。
(3)用E装置收集SO2时,气体应由(填“a”或“b”)________端进入。


 则该反应方程式中,X的化学式为:_____。
则该反应方程式中,X的化学式为:_____。