题目内容
5.金属铬(Cr)是一种重要的金属材料,它具有良好的光泽度和抗腐蚀性,常用来镀在其它金属的表面上.小柯同学为了探究铬的性质,把金属铬放入硫酸铜溶液中,发现铬表面有红色物质生成.由此他可得出的结论是( )| A. | 铬比铜活泼 | B. | 铬一定能与稀硫酸反应制得氢气 | ||
| C. | 铬不能置换出硝酸亚铁中的铁 | D. | 以上说法都正确 |
分析 根据排在前面的金属可以将排在后面的金属从其盐溶液中置换出来进行分析.
解答 解:根据“把金属铬放入硫酸铜溶液中,发现铬表面有红色物质生成”,只能说明铬比铜活泼,至于铬是否在氢之前,题中的现象不能确定,所以
A、铬比铜活泼,故A正确;
B、铬不一定能与稀硫酸反应制得氢气,故B错误;
C、无法推测铬是否能置换出硝酸亚铁中的铁,故C错误;
D、A中说法正确,故D错误.
故选:A.
点评 本题主要考查了金属活动性顺序的应用,难度不大,需要在平时加强训练.

练习册系列答案
相关题目
15.根据金属活动性顺序判断,组内物质间能够发生化学反应的是( )
| A. | 铜和稀盐酸 | B. | 铁和硫酸锌溶液 | C. | 银和稀硫酸 | D. | 锌和硝酸银溶液 |
13.酸、碱、盐是几类重要的化合物,他们之间能发生复分解反应.
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有水生成.
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象.取反应后的部分溶液加热、蒸干、得到白色固体.
以下是探究白色固体成分的实验,已知CaCl2溶液呈中性.请填写表:
实验反思:无明显现象的中和反应可借助酸碱指示剂判断反应终点.
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有水生成.
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象.取反应后的部分溶液加热、蒸干、得到白色固体.
以下是探究白色固体成分的实验,已知CaCl2溶液呈中性.请填写表:
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是用洁净玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较. | pH>7 | |
| CaCl2 |
20.下列广告用语:
①“纯净水”绝对卫生,对人体有益;
②含氟牙膏可预防龋齿;
③本饮料由天然物质配制而成,绝对不含化学物质;
④矿泉水中含钾、钠、钙、镁等多种元素,是健康饮料.
你认为正确的是( )
①“纯净水”绝对卫生,对人体有益;
②含氟牙膏可预防龋齿;
③本饮料由天然物质配制而成,绝对不含化学物质;
④矿泉水中含钾、钠、钙、镁等多种元素,是健康饮料.
你认为正确的是( )
| A. | 只有②④ | B. | 只有①④ | C. | 只有①③ | D. | 只有②③ |
10.下列图象不能正确反映对应变化关系的是( )
| A. | 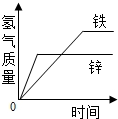 将颗粒大小相同质量相同的铁和锌分别加入到足量的同质量、同质量分数的稀盐酸中 | |
| B. | 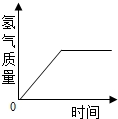 向一定量的稀硫酸中不断加入锌粒 | |
| C. | 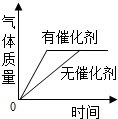 用两份等质量、等浓度的过氧化氢溶液分别制取氧气,生成气体质量的变化 | |
| D. | 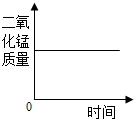 加热高锰酸钾制氧气,生成二氧化锰质量的变化 |
17. 向如表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,不能用如图曲线表示的是( )
向如表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,不能用如图曲线表示的是( )
 向如表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,不能用如图曲线表示的是( )
向如表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,不能用如图曲线表示的是( )| 甲 | 乙 | |
| A | HNO3和Mg( NO3)2的混合溶液 | KOH溶液 |
| B | Ag-Zn合金 | 稀H2SO4 |
| C | 久置空气中的铝片 | 稀盐酸 |
| D | 含有Na2CO3的NaOH溶液 | 稀HNO3 |
| A. | A | B. | B | C. | C | D. | D |
14.如图所示实验基本操作不正确的是( )
| A. | 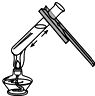 给盛有液体的试管加热 | B. |  向试管中加入液体 | ||
| C. |  闻药品气味 | D. | 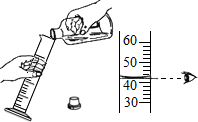 量取液体体积 |
 某化学兴趣小组设计了一组“吹气球”实验,三套装置如图所示:
某化学兴趣小组设计了一组“吹气球”实验,三套装置如图所示: