题目内容
15. 小喻为验证广告的真伪,称取碳酸钾样品(杂质为氯化钾)10克放入烧杯中,加入17.2g水待样品全部溶解后,再向其中加入稀盐酸,生成气体的质量与加入稀盐酸的质量关系如图所示,试回答:
小喻为验证广告的真伪,称取碳酸钾样品(杂质为氯化钾)10克放入烧杯中,加入17.2g水待样品全部溶解后,再向其中加入稀盐酸,生成气体的质量与加入稀盐酸的质量关系如图所示,试回答:(1)通过计算判断该广告是否虚假?(商家广告称碳酸钾含量:≥80%)
(2)加入25g稀盐酸时,烧杯中溶液的溶质质量分数是多少?
分析 碳酸钾与稀盐酸反应生成氯化钾、水和二氧化碳,由生成气体的质量与加入稀盐酸的质量关系图,当加入稀盐酸的质量为25g时,恰好完全反应,生成二氧化碳气体的质量为2.2g,由反应的化学方程式列式计算出参加反应的碳酸钾的质量、生成氯化钾的质量,进而计算出烧杯中溶液的溶质质量分数.
解答 解:设参加反应的碳酸钾的质量为x,生成氯化钾的质量为y,
K2CO3+2HCl═2KCl+H2O+CO2↑
138 149 44
x y 2.2g
(1)$\frac{138}{44}=\frac{x}{2.2g}$ x=6.9g
碳酸钾样品中碳酸钾的质量分数为$\frac{6.9g}{10g}$×100%=69%.
69%<80%,故该广告是虚假广告.
(2)$\frac{149}{44}=\frac{y}{2.2g}$ y=7.45g
加入25g稀盐酸时,烧杯中溶液的溶质质量分数是$\frac{7.45g+10g-6.9g}{10g+17.2g+25g-2.2g}$×100%=21.1%.
答:(1)该广告是虚假广告;(2)加入25g稀盐酸时,烧杯中溶液的溶质质量分数是21.1%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
5.下列有关酸和碱的说法错误的是( )
| A. | 稀硫酸滴到纸张上,在水分挥发的过程中硫酸的浓度增大也会使纸张逐渐炭化 | |
| B. | 被蚂蚁、蚊子叮咬了,涂上稀氨水或肥皂水可以止痛、消炎 | |
| C. | 配制氢氧化钠溶液时氢氧化钠固体可放在称量纸上称量 | |
| D. | 用氢氧化钠制作叶脉书签是利用了氢氧化钠的腐蚀性 |
20.下列对一些事实的解释中,不合理的是( )
| 选项 | 事实 | 解释 |
| A | 氢气可用向下排空气法收集 | 相同条件下氢气的密度比空气小 |
| B | 25m3的氧气可以装入0.024m3的钢瓶中 | 氧分子的体积变小 |
| C | 稀盐酸与稀硫酸化学性质相似 | 溶液中都含有H+ |
| D | CO2和N2都能使燃着的木条熄灭 | CO2和N2一般都不支持燃烧 |
| A. | A | B. | B | C. | C | D. | D |
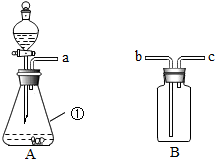 如图所示的装置适当组合可用于O2、CO2等气体的制取.
如图所示的装置适当组合可用于O2、CO2等气体的制取. 化学新材料的应用,使人们的生活质量不断提高.如图是不同年代常用的水管.
化学新材料的应用,使人们的生活质量不断提高.如图是不同年代常用的水管.
