题目内容
【题目】某化学兴趣小组在一个充满O2的密闭容器中加入一定量的碳粉,在高温条件下使其充分反应,待反应结束后,容器中的碳粉已完全消失。该小组成员对容器中反应后的气体成分进行如下探究:
(查阅资料)①CO2+2NaOH=Na2CO3+H2O; ②浓硫酸能吸收气体中的水分。
(知识回顾)碳充分燃烧和不充分燃烧的产物是不同的。
(提出猜想)
(1)小红对容器中气体的成分提出如下四种猜想,你认为猜想不合理的有_____(填字母)。
AC和CO B只有CO CCO和O2的混合气体 D只有CO2
(2)小明猜想容器中的气体可能是CO和CO2的混合气体;小强猜想可能是CO2和O2的混合气体。小明和小强均开展了以下实验探究来验证自己的猜想是否正确。
(实验探究1)小明为了验证自己的猜想,按如下图所示装置进行探究。
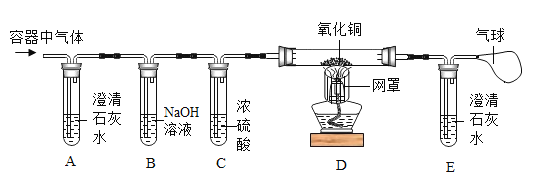
请回答下列问题:
(1)装置B中NaOH溶液的作用 _____________。
(2)若小明的猜想成立,则装置A中的实验现象是_______________,反应的化学方程式是_______________;装置D玻璃管中的实验现象是_________,反应的化学方程式是_____________。
(实验探究2)小强把小明实验中的氧化铜换成了铜丝网,并去掉E装置验证其猜想。若小强的猜想成立,则装置D中的实验现象是________________。
(反思交流)有同学认为,小强应先通入容器中气体一段时间后方可加热,你认为这样修改的原因是_________________。
【答案】AC 除去容器中气体中的二氧化碳 澄清石灰水变浑浊 CO2+Ca(OH)2═CaCO3↓+H2O 黑色粉末变为红色 CO+CuO![]() Cu+CO2 红色固体变黑 排尽玻璃管中的空气,排除空气中氧气的干扰
Cu+CO2 红色固体变黑 排尽玻璃管中的空气,排除空气中氧气的干扰
【解析】
[提出猜想]碳不是气体,CO和O2点燃的条件下会继续反应,不会共存,猜想不合理的是AC;
[实验探究1](1)由于二氧化碳能与氢氧化钠反应,所以装置B中NaOH溶液的作用是除去容器中气体中的二氧化碳;
(2)若小明的猜想成立,则装置A中的实验现象是澄清石灰水变浑浊,反应的化学方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;装置D玻璃管中的实验现象是黑色粉末变成红色,反应的化学方程式是:CO+CuO![]() Cu+CO2。
Cu+CO2。
[实验探究2]如果氧气过量,则乙容器中气体的组成是CO2和O2的混合气体;加热条件下,铜能和氧气反应生成氧化铜,所以铜丝网变黑;
[反思交流]应先通入乙中气体一段时间后方可加热,这样修改的原因是排净玻璃管中的空气,排除空气中氧气的干扰。

 名校通行证有效作业系列答案
名校通行证有效作业系列答案