题目内容
配制100g 9.2%的食盐溶液时,将食盐放于天平的右盘,游码移至0.2g处,左盘上放置的砝码质量是9g,则该学生实际称得的食盐质量是 g,若某学生在用量筒取水的体积时,仰视读书,则该学生实际配得的食盐溶液中溶质的质量分数 9.2%(填“大于”或“小于”).
(1)配制此食盐溶液,主要步骤为: 、 、 ;
(2)下列仪器不可能用到的是(填序号) ;
A.烧杯 B.漏斗 C.玻璃棒 D.量筒 E.酒精灯 F.托盘天平
(3)配制过程应选用下列哪种规格的量筒(填序号) .
A.100mL B.20mL C.50mL D.200mL.
(1)配制此食盐溶液,主要步骤为:
(2)下列仪器不可能用到的是(填序号)
A.烧杯 B.漏斗 C.玻璃棒 D.量筒 E.酒精灯 F.托盘天平
(3)配制过程应选用下列哪种规格的量筒(填序号)
A.100mL B.20mL C.50mL D.200mL.
考点:一定溶质质量分数的溶液的配制
专题:溶液、浊液与溶解度
分析:根据左物右码称量时,物体质量=砝码质量+游码质量,放反了,砝码质量=物体质量+游码质量,以及量筒读数时仰小俯大的规律进行分析.
(1)根据配制溶液的步骤进行分析;
(2)根据配制一定质量分数的溶液需要的仪器进行分析;
(3)根据所量取的水的体积选择量筒进行分析;
(1)根据配制溶液的步骤进行分析;
(2)根据配制一定质量分数的溶液需要的仪器进行分析;
(3)根据所量取的水的体积选择量筒进行分析;
解答:解:左物右码称量时,物体质量=砝码质量+游码质量,放反了,砝码质量=物体质量+游码质量,所以固体质量=9-0.2=8.8g,运用读数时仰小俯大的规律可知,俯视量取90.8mL水时,水的体积比实际体积要小,而溶质质量不变,因此所配溶液溶质质量分数偏大.
(1)配制溶质质量分数一定的溶液的基本步骤为:计算、称量、溶解;
(2)烧杯用来溶解固体,漏斗是用来过滤的,玻璃棒搅拌可以加速溶解,量筒用来量取液体的体积,酒精灯是用来加热的,托盘天平用来称量固体的质量,所以不可能用到的是:BE;
(3)配制溶液时所需水的质量为:100g-100g×9.2%=90.8g,由密度公式可得水的体积为90.8mL,所以选用的量筒是100ml的量筒量取所需要的水;
故答案为:
8.8,大于.
(1)计算、称量、溶解;
(2)BE;
(3)A;
(1)配制溶质质量分数一定的溶液的基本步骤为:计算、称量、溶解;
(2)烧杯用来溶解固体,漏斗是用来过滤的,玻璃棒搅拌可以加速溶解,量筒用来量取液体的体积,酒精灯是用来加热的,托盘天平用来称量固体的质量,所以不可能用到的是:BE;
(3)配制溶液时所需水的质量为:100g-100g×9.2%=90.8g,由密度公式可得水的体积为90.8mL,所以选用的量筒是100ml的量筒量取所需要的水;
故答案为:
8.8,大于.
(1)计算、称量、溶解;
(2)BE;
(3)A;
点评:通过本题练习,要了解溶质质量分数的计算方法,掌握了配制溶质质量分数一定的溶液的基本步骤.

练习册系列答案
相关题目
某反应的微观示意图如图(一种小球代表一种元素的原子),下列说法错误的是( )

| A、分子的种类发生变化 |
| B、反应前后原子数目没有变化 |
| C、示意图中的各物质均属于化合物 |
| D、该反应的本质是原子的重新组合 |
下列粒子中,能保持水的化学性质的是( )
| A、水分子 | B、氢原子 |
| C、氧原子 | D、氢原子和氧原子 |
在硫酸锌和硫酸铜混合液中加入过量铁粉充分反应后,过滤,留在滤纸上的是( )
| A、Cu |
| B、Zn |
| C、Zn Cu |
| D、Fe Cu |
今有四种粒子的结构示意图,下列说法不正确的是( )


| A、①表示的粒子在化学反应中易得到电子 |
| B、②③都表示阳离子 |
| C、④表示的元素属于金属元素 |
| D、它们表示四种元素 |
化学谜语:“一对兄弟,两边站起,不高不低,公平合理.”谜底是( )
| A、试管 | B、烧杯 |
| C、漏斗 | D、托盘天平 |
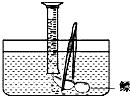 小明对妈妈杀鱼时从鱼肚内取出的鳔产生了兴趣,他确定了“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占
小明对妈妈杀鱼时从鱼肚内取出的鳔产生了兴趣,他确定了“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占 核事故时往往泄漏出污染物(具有放射性的碘原子131I).为避免核辐射,需口服100毫克(不具放射性的碘原子127I),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用.
核事故时往往泄漏出污染物(具有放射性的碘原子131I).为避免核辐射,需口服100毫克(不具放射性的碘原子127I),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用.