题目内容
13.鸡蛋壳的主要成分是碳酸钙.为了测定某鸡蛋壳中碳酸钙的质量分数,小明进行了如下实验:将洗净并干燥后的碎鸡蛋壳与足量的稀盐酸在烧杯中充分反应(假设鸡蛋壳中的其他物质,既不是与稀盐酸反应,也不溶于水).有关实验数据如下表:| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 碎鸡蛋壳的质量 | 烧杯和其中混合物的质量 |
| 150g | 12.5g | 158.1g | |
(2)计算该鸡蛋壳中碳酸钙的质量分数.
分析 反应后剩余物的总质量比反应前的减少,根据质量守恒定律知,减少的质量就是生成二氧化碳的质量,由二氧化碳的质量根据碳酸钙与盐酸反应的化学方程式可以计算出鸡蛋壳中碳酸钙的质量分数.
解答 解:(1)根据质量守恒定律,产生二氧化碳气体的质量为:150g+12.5g-158.1g=4.4g;
(2)设:该鸡蛋壳中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
x 4.4g
$\frac{100}{44}=\frac{x}{4.4g}$ 解得:x=10g
该鸡蛋壳中碳酸钙质量分数为:$\frac{10g}{12.5g}$×100%=80%
答:(1)4.4g;(2)该鸡蛋壳中碳酸钙的质量分数为80%.
点评 解答本题的关键是要知道固体质量的减少量就是生成二氧化碳的质量;根据气体的质量算出碳酸钙的质量,再计算质量分数即可.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
3.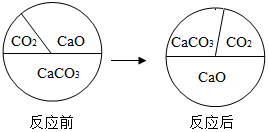 三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
 三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )| A. | 反应中CaO为催化剂 | B. | 反应后容器中氧元素质量分数不变 | ||
| C. | 该反应是化合反应 | D. | 反应后容器中固体质量不变 |
4.某校课外学习小组为探究物质燃烧需要同时满足的条件,进行探究实验(查阅资料,白磷着火点为40℃,红磷着火点为240℃),请你参与并回答下列问题:
(1)请根据下列探究实验产生的现象,得出燃烧需要同时满足的条件是?
(2)写出磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)根据生活中灭火的图示,说出下列生活中灭火的原理是?
(1)请根据下列探究实验产生的现象,得出燃烧需要同时满足的条件是?
| 实验操作现象图示 |  |  |  |
| 燃烧条件 | ① 物质具有可燃性 | ② 可燃物与氧气接触 | ③ 可燃物达到着火点 |
(3)根据生活中灭火的图示,说出下列生活中灭火的原理是?
| 灭火图示 |  用水浇灭 用水浇灭 |  砍伐树木防止火势蔓延 砍伐树木防止火势蔓延 |  |
| 灭火原理 | ① 降低周围的温度 | ② 设置隔离带即移走可燃物 | ③ 隔绝氧气 |
1.下列化学用语与所表达的意义相符合的是( )
| A. | Mg2+-镁元素的化合价为+2价 | B. | 2NO2-2个二氧化氮分子 | ||
| C. | 2N-1个氮分子由2个氮原子构成 | D. | $\stackrel{+1}{K}$-钾离子带1个单位正电荷 |
18.生活中处处充满着化学,从化学的角度看,下列说法中正确的是( )
| A. | 房屋着火,可以用水灭火,是因为降低了可燃物的着火点 | |
| B. | 室内起火,迅速打开所有门窗通风 | |
| C. | 炒菜时油锅着火,可立即加水灭火 | |
| D. | 天然气泄漏,迅速关闭阀门并开窗通风 |
20.下列符号既表示一种元素,又能表示一个原子,还能表示一种单质的是( )
| A. | H2 | B. | Mg | C. | O | D. | C |
