题目内容
20℃时:1克甲溶于10克水中正好形成饱和溶液;20克乙的饱和溶液蒸干,得4克乙固体;丙的饱和溶液的溶质质量分数为25%,则20℃时,甲、乙、丙三种物质的溶解度由大到小顺序正确的是(甲、乙、丙均不含结晶水)( )
分析:根据溶解度的概念,饱和溶液的溶质质量分数=
×100%进行分析.
| 溶解度 |
| 100g+溶解度 |
解答:解:20℃时:1克甲溶于10克水中正好形成饱和溶液,所以100g水最多溶解10g甲,所以20℃时甲的溶解度是10g;20克乙的饱和溶液蒸干,得4克乙固体说明16g水中最多溶解4g乙,则100g水中最多溶解25g,所以乙的溶解度是25g,设丙的溶解度是X,由于丙的饱和溶液的溶质质量分数为25%,即
×100%=25%,解得x=33.33g,所以20℃时,甲、乙、丙三种物质的溶解度由大到小顺序正确的是丙>乙>甲.
故选:C.
| x |
| 100g+x |
故选:C.
点评:解答本题关键是要知道溶解度的四要素,熟悉溶解度的计算方法考虑.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
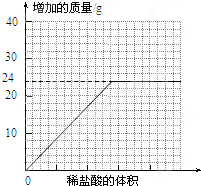
某课外活动小组在春游时,带回了几块石灰石样品.为了检测样品中碳酸钙的含量.甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定(样品的杂质不溶于水,且不与盐酸反应)测定的数据见下表:
试回答:
(1)样品中碳酸钙的质量分数是______.
(2)10.0g样品与足量的稀盐酸反应后可产生二氧化碳多少克?(写出计算过程.计算结果精确到小数点后两位)
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品的质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸的质量(g) | 20.0 | 30.0 | 45.0 | 50.0 |
| 剩余固体的质量(g) | 6.0 | 4.0 | 1.0 | 1.0 |
(1)样品中碳酸钙的质量分数是______.
(2)10.0g样品与足量的稀盐酸反应后可产生二氧化碳多少克?(写出计算过程.计算结果精确到小数点后两位)