题目内容
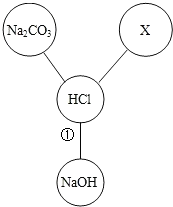 小红同学在学习盐酸的化学性质时,归纳出了盐酸与其它物质相互反应的关系,如图(图中“-”表示相连的两种物质能发生反应).
小红同学在学习盐酸的化学性质时,归纳出了盐酸与其它物质相互反应的关系,如图(图中“-”表示相连的两种物质能发生反应).(1)若X是与其它三种不同类别的化合物,则X可以是
(2)根据如图所示物质间的关系,写出①反应的化学方程式:
(3)当X是单质时,请写出X与稀盐酸反应的化学方程式:
考点:酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)根据酸的化学性质,酸能与碱反应,酸能与盐反应,酸能与碱性氧化物反应可解答此题;
(2)根据复分解反应发生的实质,可以书写化学方程式;
(3)根据酸能与活泼金属单质反应解答.
(2)根据复分解反应发生的实质,可以书写化学方程式;
(3)根据酸能与活泼金属单质反应解答.
解答:解:(1)因为我们学过酸的化学性质,酸能与活泼金属、碱、盐、碱性氧化物反应,又因为氢氧化钠属于碱,碳酸钠属于盐,因此X应该是碱性氧化物,所以我们可以选择学过的最常见的碱性氧化物氧化铁、氧化铜等;
(2)氢氧化钠与盐酸反应生成氯化钠和水,化学方程式为:NaOH+HCl=NaCl+H2O;
(3)酸能与活泼金属单质反应,当X是单质时,可以是铁、锌或铝等,化学方程式为:Fe+2HCl=FeCl2+H2↑.
故答案为:(1)CuO;
(2)NaOH+HCl=NaCl+H2O;
(3)Fe+2HCl=FeCl2+H2↑.
(2)氢氧化钠与盐酸反应生成氯化钠和水,化学方程式为:NaOH+HCl=NaCl+H2O;
(3)酸能与活泼金属单质反应,当X是单质时,可以是铁、锌或铝等,化学方程式为:Fe+2HCl=FeCl2+H2↑.
故答案为:(1)CuO;
(2)NaOH+HCl=NaCl+H2O;
(3)Fe+2HCl=FeCl2+H2↑.
点评:此题主要考查了酸的化学性质和复分解反应发生的实质,是中考考试的重点,侧重学生的基础知识,考查系统全面.

练习册系列答案
 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案
相关题目
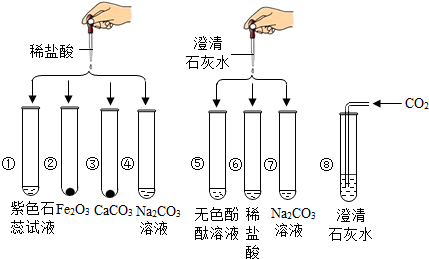
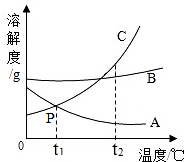 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答:


 ”、“
”、“ ”、“
”、“ ”分别表示氧元素和另外两种元素的原子,则下列表示的气体物质中,属于氧化物的是( )
”分别表示氧元素和另外两种元素的原子,则下列表示的气体物质中,属于氧化物的是( )