题目内容
上海世博会上,100辆燃料电池观光汽车活跃在世博会园区,他们靠氢气和氧气反应提供能量,由于它们“喝”的是氢气,产生的是水,真正实现了“零排放”.若燃烧2.0g氢气,需要多少体积空气(标准状况下氧气密度1.43g/L,氧气占空气总体积21%,结果保留一位小数)?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:氢气燃烧生成水,根据氢气的质量可以计算反应的氧气的质量;
根据氧气的密度可以计算氧气的体积,根据氧气的体积及其在空气中的含量可以计算需要空气的体积.
根据氧气的密度可以计算氧气的体积,根据氧气的体积及其在空气中的含量可以计算需要空气的体积.
解答:解:设需要氧气的质量为x,
2H2+O2
2H2O,
4 32
2.0g x
=
,
x=16g,
氧气的体积为:16g÷1.43g/L=11.2L,
需要空气的体积为:11.2L÷21%=53.3L,
答:燃烧2.0g氢气,需要53.3L空气.
2H2+O2
| ||
4 32
2.0g x
| 4 |
| 2.0g |
| 32 |
| x |
x=16g,
氧气的体积为:16g÷1.43g/L=11.2L,
需要空气的体积为:11.2L÷21%=53.3L,
答:燃烧2.0g氢气,需要53.3L空气.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
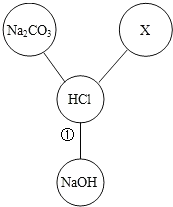 小红同学在学习盐酸的化学性质时,归纳出了盐酸与其它物质相互反应的关系,如图(图中“-”表示相连的两种物质能发生反应).
小红同学在学习盐酸的化学性质时,归纳出了盐酸与其它物质相互反应的关系,如图(图中“-”表示相连的两种物质能发生反应).