题目内容
19. 某兴趣小组围绕“燃烧条件”这一主题开展如下探究活动,请你参与.
某兴趣小组围绕“燃烧条件”这一主题开展如下探究活动,请你参与.【实验内容】
①用棉花分别蘸酒精和水,放在酒精灯上加热片刻,观察现象.
②取一小块乒乓球碎片和滤纸碎片,分别用坩埚钳夹住,放在酒精灯火焰上加热,观察两种物质都能燃烧.
③从乒乓球和滤纸上各剪下一小片(同样大小),如图1所示分开放在一片薄铜片的两侧,加热铜片的中部,观察现象.
【分析讨论】
(1)进行实验①时,如果在酒精灯上加热时间较长,两个棉花球都会燃烧起来. 其中蘸水的棉花球燃烧的原因是棉花中的水蒸发后,温度达到棉花的着火点,并与氧气接触,引起燃烧;
(2)进行实验②的目的是为了证明这两种物质都是可燃物,实验③看到的现象是乒乓球碎片先燃烧,滤纸碎片后燃烧,这两个实验的对比说明,燃烧的条件之一是可燃物燃烧时温度需要达到着火点.
【反思与应用】
(3)毕业联欢会上,小明表演了一个小魔术:将一根粗铜丝绕成线圈,罩在蜡烛火焰上(如图2所示),观察到火焰缓缓熄灭,他再将铜圈加热后罩在蜡烛火焰上,观察到蜡烛照常燃烧,请你分析原因是:前者是因为铜丝吸热使蜡烛温度降到着火点以下;而后者热铜丝不会吸热,所以可以正常燃烧(其他合理答案均可).
分析 根据燃烧的条件(燃烧需要同时满足三个条件:①可燃物、②氧气或空气、③温度要达到着火点),进行分析解答本题;
燃烧着的物质熄灭了,一定是满足了灭火的原理:清除可燃物或使可燃物与其他物品隔离、隔绝氧气(或空气)或使温度降到着火点以下.据此答题.
解答 解:(1)用棉花分别蘸酒精和水,放在酒精灯火焰上加热片刻,如果在酒精灯上加热时间较长,蘸水的棉花球也会燃烧起来,其原因是 棉花中的水蒸发后,温度达到棉花的着火点,并与氧气接触,引起燃烧.故填:棉花中的水蒸发后,温度达到棉花的着火点,并与氧气接触,引起燃烧;
(2)物质受热时,如果能够燃烧,说明是可燃物,因此用坩埚钳夹住乒乓球碎片和滤纸碎片放在酒精灯的火焰上加热,其目的是证明乒乓球碎片和滤纸碎片都是可燃物.乒乓球碎片的着火点比滤纸碎片的着火点低,把它们分开放在薄铜片上加热时,乒乓球碎片先燃烧,说明燃烧的条件之一是温度达到可燃物的着火点.故填:这两种物质都是可燃物;乒乓球碎片先燃烧,滤纸碎片后燃烧;可燃物燃烧时温度需要达到着火点;
(3)蜡烛能够熄灭一定是缺少了燃烧的条件,铜圈罩在蜡烛火焰上,既没有清除可燃物,也没有隔绝氧气,只能是温度降低到了着火点以下;后者不熄灭是因为铜圈加热后不在吸收热量,所以蜡烛不会熄灭.
故答案为:前者是因为铜丝吸热使蜡烛温度降到着火点以下;而后者热铜丝不会吸热,所以可以正常燃烧(其他合理答案均可).
点评 可燃物燃烧的条件是:与氧气接触,温度达到可燃物的着火点,二者必须同时具备,缺一不可,本实验中,没有涉及氧气是否参加的对比实验,要注意这一点.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
9. 为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,李铭和同学们通过测定反应后溶液的pH,得到如图所示的pH曲线,请回答:
为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,李铭和同学们通过测定反应后溶液的pH,得到如图所示的pH曲线,请回答:
(1)由图可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,李铭取了a、b、c三处反应后的溶液于三个烧杯中,却忘了作标记,请你设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了以下方案:
【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑反应物是否有剩余.
 为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,李铭和同学们通过测定反应后溶液的pH,得到如图所示的pH曲线,请回答:
为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,李铭和同学们通过测定反应后溶液的pH,得到如图所示的pH曲线,请回答:(1)由图可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,李铭取了a、b、c三处反应后的溶液于三个烧杯中,却忘了作标记,请你设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了以下方案:
| 实验步骤 | 实验现象 | 实验结论 |
| 另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液. | 只产生白色沉淀 | 该样品为b处溶液. |
| 先生成气体,后生成白色沉淀 | 该样品为c处溶液,并推知溶液中的阳离子有Ca2+、H+. |
14.为达到实验目的,下列实验方案或结论不正确的是( )
| 选项 | 实验目的 | 实验方案或结论 |
| A | 除去KCl溶液中混有的 K2 SO4 | 加入过量的BaCl2溶液 |
| B | 鉴别①CuSO4溶液②稀H2SO4③NaCl溶液④NaOH溶液 | 不用其它任何试剂就能鉴别,且鉴别的顺序为①④②③或①④③② |
| C | 使Fe(OH)3一步转化为 FeCl3 | 唯一的方法只能加入稀盐酸 |
| D | 鉴别NaCl溶液、NaOH溶液和 BaCl2溶液 | 各取少量于试管中,分别滴加 CuSO4溶液,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
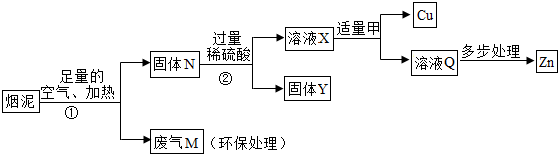
11.管道烟泥中含有某些单质,其中Cu约占10.3%、Zn约占5.0%、S约占1.2%.在加热的条件下,Zn、Cu都可以与氧气反应生成相应的金属氧化物;现欲回收铜和锌,并对硫进行环保处理,主要步骤如下图所示.下列说法正确的是( )

| A. | ②、③中的操作均包含过滤 | |
| B. | 溶液X中ZnSO4的质量大于CuSO4的质量 | |
| C. | 步骤①中即使空气不足量,也不会导致锌的回收率降低 | |
| D. | ①产生的废气M可以用石灰乳处理,反应方程式是SO2+Ca(OH)2═CaSO4+H2O |
