题目内容
如何用化学方法除去下列物质中的杂质 (括号中为杂质 ),写出有关的化学反应方程式:
(1)CaO(CaCO3)
(2)Cu(Fe)
(3)FeSO4溶液(CuSO4)
(4)CO2(CO)
(5)CO(CO2) .
(1)CaO(CaCO3)
(2)Cu(Fe)
(3)FeSO4溶液(CuSO4)
(4)CO2(CO)
(5)CO(CO2)
考点:物质除杂或净化的探究,常见气体的检验与除杂方法,金属的化学性质,盐的化学性质
专题:物质的分离、除杂、提纯与共存问题
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:(1)碳酸钙在高温下分解生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CaCO3
CaO+CO2↑.
(2)根据金属活动性顺序,铁能和酸反应,铜和酸不反应,故可用盐酸或稀硫酸除去铁,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+2HCl=FeCl2+H2↑(合理即可).
(3)要除去FeSO4溶液中的CuSO4,实质就是除去铜离子,可利用CuSO4溶液与过量的铁粉应生成硫酸亚铁溶液和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
(4)根据一氧化碳和二氧化碳的化学性质,一氧化碳能与灼热的氧化铜反应生成铜和二氧化碳,二氧化碳不与氧化铜不反应,故可将混合气体通过灼热的氧化铜,反应的化学方程式为:CO+CuO
Cu+CO2.
(5)根据一氧化碳和二氧化碳的化学性质,CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
故答案为:(1)CaCO3
CaO+CO2↑;(2)Fe+2HCl=FeCl2+H2↑(合理即可);(3)Fe+CuSO4═FeSO4+Cu;(4)CO+CuO
Cu+CO2;(5)CO2+2NaOH═Na2CO3+H2O.
| ||
(2)根据金属活动性顺序,铁能和酸反应,铜和酸不反应,故可用盐酸或稀硫酸除去铁,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+2HCl=FeCl2+H2↑(合理即可).
(3)要除去FeSO4溶液中的CuSO4,实质就是除去铜离子,可利用CuSO4溶液与过量的铁粉应生成硫酸亚铁溶液和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
(4)根据一氧化碳和二氧化碳的化学性质,一氧化碳能与灼热的氧化铜反应生成铜和二氧化碳,二氧化碳不与氧化铜不反应,故可将混合气体通过灼热的氧化铜,反应的化学方程式为:CO+CuO
| ||
(5)根据一氧化碳和二氧化碳的化学性质,CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
故答案为:(1)CaCO3
| ||
| ||
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.
除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为
除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
小分子团水是航天员专用水,具有饮用量少、体内储留时间长、排放量少等特点.下列关于小分子团水的说法正确的是( )
| A、水分子的化学性质被改变了 |
| B、小分子团水中水分子间没有间隙 |
| C、小分子团中的水分子停止了运动 |
| D、小分子团水的物理性质与普通水不同 |
要除去FeSO4溶液中少量的H2SO4,可加入的物质是( )
①铁粉 ②氧化铁 ③氧化亚铁 ④氢氧化铁 ⑤氢氧化亚铁.
①铁粉 ②氧化铁 ③氧化亚铁 ④氢氧化铁 ⑤氢氧化亚铁.
| A、①②③ | B、②③④ |
| C、①③⑤ | D、②③⑤ |
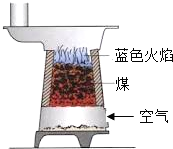 煤燃烧时上方会出现蓝色火焰(如图)是CO燃烧产生的.请用化学方程式表示此反应:
煤燃烧时上方会出现蓝色火焰(如图)是CO燃烧产生的.请用化学方程式表示此反应: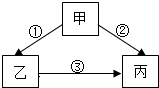 甲、乙、丙是初中化学中常见的物质,其中一种物质为单质,另外两种物质组成元素相同.其转化关系如图所示:
甲、乙、丙是初中化学中常见的物质,其中一种物质为单质,另外两种物质组成元素相同.其转化关系如图所示: