题目内容
在一定温度下,将甲、乙、丙三种物质溶于水配成饱和溶液:
10g甲溶于40g水中;5g乙配成15g溶液;丙溶液中丙的质量分数为25%.则三种物质的溶解度由大到小的顺序是[
]|
A .甲、乙、丙 |
B .丙、乙、甲 |
|
C .乙、丙、甲 |
D .乙、甲、丙 |
答案:C
解析:
提示:
解析:
|
解析:本题综合了根据不同条件求溶解度的计算.甲物质的溶解度是根据溶质和溶剂的质量计算;乙物质的溶解度是根据饱和溶液的溶质质量计算;丙物质的溶解度是根据溶质的质量分数计算. 设甲的溶解度为 x,则
 ; ;
设乙的溶解度为 y,则
 ; ;
所以溶解度从大到小的顺序为乙、丙、甲. 或者直接换算成溶质与溶剂的质量比,比值越大则溶解度也越大,具体计算如下:
 
所以乙>丙>甲. |
提示:
|
点拨:此题考查了同学们时溶解度概念的理解及应用.如果给出溶质、溶剂或溶液的质量,一定要换算成 100g溶剂中溶解的溶质质量,即为该温度下的溶解度,即 .如果给出饱和溶液的质量分数为p%,则 .如果给出饱和溶液的质量分数为p%,则 ,或者直接换算成溶质质量和溶剂质量之比,比值越大,其时应的溶解度越大. ,或者直接换算成溶质质量和溶剂质量之比,比值越大,其时应的溶解度越大. |

练习册系列答案
相关题目
根据信息回答问题:
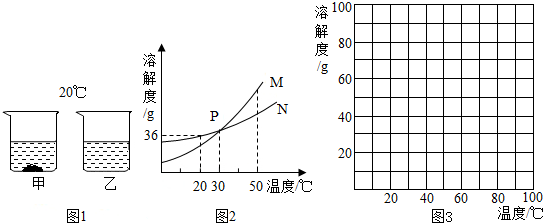
(1)20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,甲、乙两种固体物质溶解度曲线如图2,结合图示回答下列问题:

①______℃时两种物质的溶解度相等.
②图2中表示乙的溶解度曲线是______.
③20℃时将19g物质N溶解在50g水里所得溶液的浓度是______(精确到0.1%).
(2)下表是NaCl和KNO3在不同温度时的溶解度:
| 温度(℃) | 0 | 10 | 20 | 40 | 50 | 60 | 70 |
| KNO3 | 13.3 | 20.9 | 31.6 | 64 | 85.5 | 110 | 138 |
| NaCl | 35.7 | 35.8 | 36 | 36.6 | 37 | 37.5 | 37.8 |
②若通过降温的方法从NaCl和KNO3的混合溶液中提纯KNO3后,对剩余溶液及析出的晶体描述正确的是______.
A.剩余溶液一定是KNO3饱和溶液
B.剩余溶液一定是NaCl不饱和溶液
C.上述方法可以将两者完全分离
D.析出的晶体中只含有KNO3
③在一定温度下,将含69g KNO3、18g NaCl的混合物完全溶解在50g水中,改变温度使KNO3析出,NaCl不析出,则温度范围是______(硝酸钾和氯化钠溶解度互不影响).