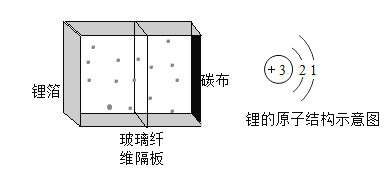
题目内容
铜锈的主要成分是碱式碳酸铜。碱式碳酸铜受热分解的化学方程式为: ,下列说法正确的是
,下列说法正确的是
A.反应前后固体物质中铜元素的质量分数不变
B.碱式碳酸铜中铜原子和氧原子的个数比为2∶3
C.X是相对分子质量最小的氧化物
D.加热Cu2(OH)2CO3的实验装置和实验室制取CO2的发生装置相同
空气中氧气含量测定的再认识。
(实验回顾)图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。
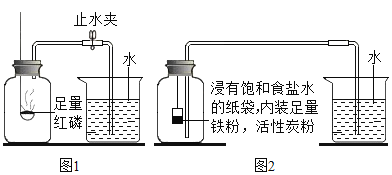
(1)写出红磷燃烧的化学方程式____________。
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内___________减小,烧杯中水倒吸到集气瓶。若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
(问题提出)有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大。
(实验改进)
Ⅰ.根据铁在空气中生镑的原理设计图2实验装置,再次测定空气中氧气含量。装置中饱和食盐水、活性炭会加速铁生锈。
Ⅱ.测得实验数据如表
测量项目 | 实验前 | 试验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
(交流表达)
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式________________。
(2)根据表数据计算,改进实验后测得的空气中氧气的体积分数是_______(计算结果精确到0.1%)。
(3)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是:①_______________;②_____________。
为了测定蜡烛中碳、氢两种元素的质量比,某化学兴趣小组设计了如下图所示的实验装置,实验步骤如下:先分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量。按图示连接好仪器,点燃蜡烛,同时从a导管口抽气,一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量,实验数据如下表所示:(浓硫酸有吸水性,氢氧化钠和氧化钙既可吸水,又可吸收二氧化碳)
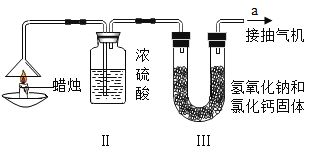
蜡烛 | 装置Ⅱ | 装置Ⅲ | |
反应前的质量/g | 15.8 | 182.3 | 212.2 |
反应后的质量/g | 14.4 | 184.1 | 216.6 |
(1)该实验中测得水的质量为_______g,二氧化碳的质量为_______g。
(2)由该实验数据计算,蜡烛中碳、氢元素的质量之比为_______。
(3)装置Ⅱ和装置Ⅲ的顺序能否颠倒?_______(填“能”或“不能”)。
(4)理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛减小的质量,其原因是_______。
(5)该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?____(填“能”或“不能”),理由是____。


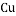
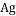

 ”代表碳原子,“
”代表碳原子,“ ”代表氢原子。试根据分子模型写出对二甲苯的化学式__________________;
”代表氢原子。试根据分子模型写出对二甲苯的化学式__________________;