题目内容
15.配置一定质量分数的NaOH溶液,部分实验如图所示:
(1)若要配置10%的NaOH溶液100g,需NaOH固体10g,水90mL;
(2)操作A中一处明显错误,应改正为应将氢氧化钠放在烧杯中称量;
(3)若操作B中读取量筒中液体溶液体积时俯视,会导致配置溶液的质量分数偏大(填“偏大”“偏小”)
分析 (1)根据溶质质量分数公式进行解答;
(2)根据溶液配制的注意事项进行解答;
(3)根据读取量筒中液体溶液体积时俯视,会导致水的体积偏小进行解答.
解答 解:(1)配置10%的NaOH溶液100g,需NaOH固体的质量=100g×10%=10g,水的质量=100g-10g=90g,所以水的体积为90mL;故填:10;90;
(2)氢氧化钠具有强烈的腐蚀性,所以应将氢氧化钠放在烧杯中称量;故填:应将氢氧化钠放在烧杯中称量;
(3)读取量筒中液体溶液体积时俯视,会导致水的体积偏小,所以会导致配置溶液的质量分数偏大.故填:偏大.
点评 该题以溶液配制为载体,考查了溶液中计算、操作的步骤、错误或不规范操作引起的溶质质量变化解答时要看清图示,结合具体知识点进行解答.

练习册系列答案
相关题目
6.通常情况下,几种物质的着火点如表
根据表中所给信息和所学相关知识判断,下列说法错误的是( )
| 物质 | 白磷 | 红磷 | 木炭 | 无烟煤 |
| 着火点/℃ | 40 | 240 | 320-370 | 700-750 |
| A. | 白磷、红磷、木材、酒精都是可燃物 | |
| B. | 降低可燃物的着火点可以达到灭火的目的 | |
| C. | 实验时,用于吸干白磷的滤纸片不能丢在废纸篓里 | |
| D. | 红磷燃烧属于置换反应 |
10.下列不属于中和反应在生产生活中的应用的是( )
| A. | 用石灰粉改良酸性土壤 | B. | 往造纸厂排放的碱溶液中加盐酸 | ||
| C. | 含氢氧化铝的胃药治疗盐酸过多 | D. | 硫酸铜与碱石灰配置波尔多液 |
7.一个碳原子的质量是1.993×10-26Kg,碳的相对原子质量为( )
| A. | 12g | B. | $\frac{1}{12}$ | ||
| C. | 12 | D. | $\frac{1.993×1{0}^{-26}Kg}{12}$ |
4.已知氯化铁溶液有如下性质:和铜反应生成氯化亚铁和氯化铜;和铁反应生成氯化亚铁.请根据上述信息完成有一包铁粉和铜粉混合物,为确定其组成将不同质量的样品分别放入FeCl3溶液中(其他用品略),实验数据记录如下
下列结论错误的是( )
| 组别 | ① | ② | ③ | ④ |
| 溶液中FeCl3的质量(g) | 65 | 65 | 65 | 65 |
| 混合粉末质量/g | 6 | 13.2 | 24 | 36 |
| 反应后剩余固体质量/g | 0 | 1.28 | 12.8 | 24.8 |
| A. | 第①组:反应后溶液中含有32.5克FeCl3 | |
| B. | 第②组:在反应后溶液中放入一根铁丝,铁钉表面无变化 | |
| C. | 第③组:剩余固体中滴加盐酸无气泡产生 | |
| D. | 第④组:剩余固体中铁与铜的物质的量之比为1:3 |
5.现代生活中金属腐蚀生锈造成了大量的资源和能源浪费,每年都会形成巨额的经济损失.下列措施中,不能防止铁制品锈蚀的是( )
| A. | 喷漆 | B. | 镀一层耐腐蚀的金属 | ||
| C. | 涂油 | D. | 存放在潮湿的空气中 |
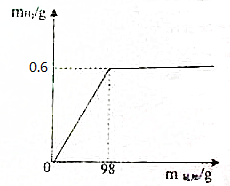 某研究性学习小组为测定铜锌合金中铜的质量分数,进行如下实验:取合金40g,加入足量的稀硫酸,产生的气体与所加稀硫酸的质量关系如图所示的曲线图,回答下列问题:
某研究性学习小组为测定铜锌合金中铜的质量分数,进行如下实验:取合金40g,加入足量的稀硫酸,产生的气体与所加稀硫酸的质量关系如图所示的曲线图,回答下列问题: