题目内容
实验室制下列三种气体
A.O2:2KClO3
2KCl+3O2↑
B.CO2:
C.Cl2:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
说明:Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体.
(1)写出制CO2的反应方程式
(2)有下列三种制气装置两种集气装置
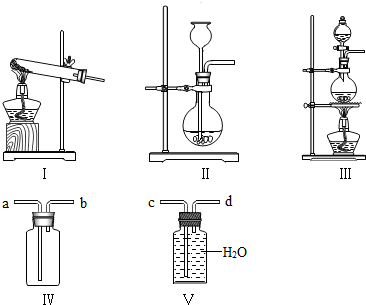
①制取CO2应选取的发生装置是 ,应选用Ⅲ装置制取的气体是 ;
②用Ⅳ装置收集Cl2应从 口进气,
上述三种气体中,能用Ⅴ装置收集的气体有 ,应从 口进气.
(3)A中制O2后,从剩余固体中分离出MnO2的操作有 (不需烘干),所用到的玻璃仪器有 .
(4)用100g 36.5%的浓盐酸与足量MnO2混合加热,理论上能制得Cl2的质量为 g,而实际收集到的Cl2质量远远小于这个数值,若操作正确,装置不漏气,则可能的原因有 , (任写两个)
A.O2:2KClO3
| ||
| △ |
B.CO2:
C.Cl2:MnO2+4HCl(浓)
| ||
说明:Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体.
(1)写出制CO2的反应方程式
(2)有下列三种制气装置两种集气装置

①制取CO2应选取的发生装置是
②用Ⅳ装置收集Cl2应从
上述三种气体中,能用Ⅴ装置收集的气体有
(3)A中制O2后,从剩余固体中分离出MnO2的操作有
(4)用100g 36.5%的浓盐酸与足量MnO2混合加热,理论上能制得Cl2的质量为
考点:常用气体的发生装置和收集装置与选取方法,混合物的分离方法,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.制取CO2应选取的发生装置是Ⅱ,不需要加热;应选用Ⅲ装置制取的气体是氯气;用Ⅳ装置收集Cl2应从长管进入,因为氯气的密度比空气的密度大;A中制O2后,从剩余固体中分离出MnO2的操作有溶解、过滤,过滤用到的玻璃仪器有:烧杯、玻璃棒、漏斗;根据化学方程式的计算要准确,而实际收集到的Cl2质量远远小于这个数值,若操作正确,装置不漏气,则可能的原因有:容器内有残留的部分氯气没有排出来;Cl2部分溶于水;或随着反应进行,盐酸浓度变小,MnO2与稀盐酸不反应,该反应停止等.
解答:解:(1)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,配平即可;
故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)制取CO2应选取的发生装置是Ⅱ,不需要加热;应选用Ⅲ装置制取的气体是氯气;用Ⅳ装置收集Cl2应从长管进入,因为氯气的密度比空气的密度大;
故答案为:①Ⅱ;Cl2;②a;O2;d;
(3)A中制O2后,从剩余固体中分离出MnO2的操作有溶解、过滤,过滤用到的玻璃仪器有:烧杯、玻璃棒、漏斗;
故答案为:溶解、过滤;烧杯、玻璃棒、漏斗;
(4)100g×36.5%=36.5g,设生成氯气的质量为x
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
146 71
36.5g x
=
x=17.75g
实际收集到的Cl2质量远远小于这个数值,若操作正确,装置不漏气,则可能的原因有:容器内有残留的部分氯气没有排出来;Cl2部分溶于水;或随着反应进行,盐酸浓度变小,MnO2与稀盐酸不反应,该反应停止等;
故答案为:17.75;容器内有残留的部分氯气没有排出来;Cl2部分溶于水;或随着反应进行,盐酸浓度变小,MnO2与稀盐酸不反应,该反应停止(合理均可);
故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)制取CO2应选取的发生装置是Ⅱ,不需要加热;应选用Ⅲ装置制取的气体是氯气;用Ⅳ装置收集Cl2应从长管进入,因为氯气的密度比空气的密度大;
故答案为:①Ⅱ;Cl2;②a;O2;d;
(3)A中制O2后,从剩余固体中分离出MnO2的操作有溶解、过滤,过滤用到的玻璃仪器有:烧杯、玻璃棒、漏斗;
故答案为:溶解、过滤;烧杯、玻璃棒、漏斗;
(4)100g×36.5%=36.5g,设生成氯气的质量为x
MnO2+4HCl(浓)
| ||
146 71
36.5g x
| 146 |
| 71 |
| 36.5g |
| x |
实际收集到的Cl2质量远远小于这个数值,若操作正确,装置不漏气,则可能的原因有:容器内有残留的部分氯气没有排出来;Cl2部分溶于水;或随着反应进行,盐酸浓度变小,MnO2与稀盐酸不反应,该反应停止等;
故答案为:17.75;容器内有残留的部分氯气没有排出来;Cl2部分溶于水;或随着反应进行,盐酸浓度变小,MnO2与稀盐酸不反应,该反应停止(合理均可);
点评:本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、过滤操作和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
