题目内容
4.工业上常用红锌矿(主要含ZnO)和稀硫酸为原料制取硫酸锌作木材防腐剂(化学反应方程式为H2SO4+ZnO═ZnSO4+H2O),现用含氧化锌81%的红锌矿50Kg与足量的稀硫酸反应,来制取16%的硫酸锌溶液.(最后结果保留1位小数)(1)硫酸锌中锌元素、硫元素和氧元素间的质量比为65:32:64.
(2)制得的硫酸锌溶液质量是多少?
分析 (1)根据化合物中各元素的质量比,即为化学式中各原子的相对原子质量和的比进行分析;
(2)根据化学方程式和题中的数据减小计算.
解答 解:(1)硫酸锌中锌元素、硫元素和氧元素间的质量比为65:32:(16×4)=65:32:64;
(2)设生成硫酸锌溶液的质量为x
ZnO+H2SO4═ZnSO4+H2O,
81 161
81%×50kg x×16%
$\frac{81}{81%×50kg}$=$\frac{161}{x×16%}$
x=503.1kg
故答案为:(1)65:32:64;
(2)503.1Kg.
点评 本题主要考查学生化学式计算、溶液计算和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目
15.用实验比较铜、锌、银的金属活动性,最好的方法是选用下列试剂中的( )
| A. | CuSO4溶液 | B. | NaOH溶液 | C. | 稀硫酸 | D. | ZnSO4溶液 |
12.下列属于物理变化的是( )
| A. | 火箭发射 | B. | 光合作用 | C. | 冰雪融化 | D. | 葡萄酿酒 |
9.下列有关物质组成的说法错误的是( )
| A. | 葡萄糖(C6H12O6)是一种有机物 | |
| B. | 煤是混合物,燃烧后生成二氧化碳、二氧化硫和二氧化氮 | |
| C. | 酒精、天然气、煤气都含有碳、氢元素,都可以作燃料 | |
| D. | 黄铜、硬铝、钢铁都是金属合金,与非金属无关 |
3.根据下列装置图回答问题(所有装置图用序号表示)
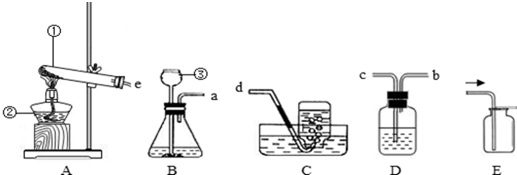
(1)写出中标号的仪器名称:①试管,②酒精灯,③长颈漏斗.
(2)利用装置A可制得的常见气体是氧气(或O2),该反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
(3)制取并收集CO2气体可选用装置BE,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑ 检验CO2可用D装置,气体从c(填b或c)端进入.
(4)查阅以下资料回答下列问题:
①实验室制取氯气时是不可以(填“可以”或“不可以”)采用装置A的,因为制取氯气是利用固体与液体混合的反应.
②实验室收集氯气是不可以采用装置C的(水槽中是水),理由是氯气可溶于水.

(1)写出中标号的仪器名称:①试管,②酒精灯,③长颈漏斗.
(2)利用装置A可制得的常见气体是氧气(或O2),该反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
(3)制取并收集CO2气体可选用装置BE,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑ 检验CO2可用D装置,气体从c(填b或c)端进入.
(4)查阅以下资料回答下列问题:
| 物质 | 制取气体的药品 | 制取气体的反应条件 | 气体的物理性质 |
| 氯气 | MnO2固体和浓盐酸 | 需要加热 | 可溶于水,密度比空气大 |
②实验室收集氯气是不可以采用装置C的(水槽中是水),理由是氯气可溶于水.
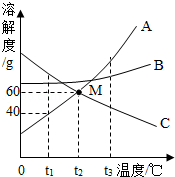 如图是常见固体物质的溶解度曲线,根据图示回答:
如图是常见固体物质的溶解度曲线,根据图示回答:



