题目内容
7.氯化钠是生活中常用的调味品,其溶解度如表所示.下列说法正确的是( )| 温度/℃ | 0 | 20 | 40 | 60 |
| 溶解度/g | 35.7 | 36.0 | 36.6 | 37.3 |
| A. | 将氯化钠饱和溶液蒸发溶剂后恢复至原温度,有结晶析出 | |
| B. | 20℃时,氯化钠饱和溶液中溶质的质量分数是36.0% | |
| C. | 40℃和60℃的两份氯化钠溶液,所含溶质的质量不可能相等 | |
| D. | 60℃时,100克水中溶解的氯化钠越多溶解度就越大 |
分析 A.根据饱和溶液蒸发溶剂会析出晶体来分析;
B.根据饱和溶液中溶质的质量分数与溶解度的关系来分析;
C.根据未知溶液的质量与状态来分析;
D.根据影响固体溶解度的因素来分析.
解答 解:A.给氯化钠的饱和溶液蒸发溶剂再恢复到原来的温度,则原来溶解在这部分溶剂中的溶质就会结晶析出,故正确;
B.由表格数据可知,20℃时,氯化钠的溶解度为36.0g,即该温度下的100g水中溶解36.0g氯化钠就达到饱和,此时饱和溶液中溶质的质量分数为$\frac{36.0g}{36.0g+100g}×100%$≈26.5%,故错误;
C.没有说明两份溶液的质量大小,也没有说明两份溶液是否饱和,所以无法判断所含溶质的质量关系,故错误;
D.60℃时,氯化钠的溶解度为37.3g,也就是在该温度下100克水中最多能溶解37.3g的氯化钠,故错误.
故选A.
点评 本题难度不是很大,主要考查了固体的溶解度的意义,及根据固体的溶解度以及受温度影响情况来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
17.金属钛(Ti)抗腐蚀性能好,露置于空气中数年仍光亮如初.工业上常用以金红石(主要成分是TiO2)为原料生产金属钛,在生产过程中发生此反应:TiO2+X═Ti+CO2↑,下列说法不正确的是( )
| A. | X的化学式是C | B. | 该反应是置换反应 | ||
| C. | TiO2中钛元素的化合价为+4 | D. | TiO2是该反应的还原剂 |
15. 2016年,美国诺贝尔化学奖获得者乔治•欧拉率领团队,首次采用金属钌做催化剂,将从空气中捕获的二氧化碳直接转化为甲醇燃料,转化率高达79%,该研究向通往未来“甲醇经济”迈出了重要一步,如图是钌元素在元素周期表中的信息,下列说法正确的是( )
2016年,美国诺贝尔化学奖获得者乔治•欧拉率领团队,首次采用金属钌做催化剂,将从空气中捕获的二氧化碳直接转化为甲醇燃料,转化率高达79%,该研究向通往未来“甲醇经济”迈出了重要一步,如图是钌元素在元素周期表中的信息,下列说法正确的是( )
 2016年,美国诺贝尔化学奖获得者乔治•欧拉率领团队,首次采用金属钌做催化剂,将从空气中捕获的二氧化碳直接转化为甲醇燃料,转化率高达79%,该研究向通往未来“甲醇经济”迈出了重要一步,如图是钌元素在元素周期表中的信息,下列说法正确的是( )
2016年,美国诺贝尔化学奖获得者乔治•欧拉率领团队,首次采用金属钌做催化剂,将从空气中捕获的二氧化碳直接转化为甲醇燃料,转化率高达79%,该研究向通往未来“甲醇经济”迈出了重要一步,如图是钌元素在元素周期表中的信息,下列说法正确的是( )| A. | 钌元素的相对原子质量为101.1g | B. | 钌原子核内中子数是44 | ||
| C. | 钌原子的核外电子数是44 | D. | 钌属于非金属元素 |
12.如图所示的基本实验操作中错误的是( )
| A. | 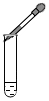 滴加少量液体 | B. | 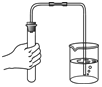 检查装置气密性 | C. | 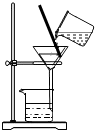 过滤液体 | D. | 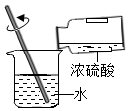 稀释浓硫酸 |
16.1828年,德国化学家维勒通过蒸发氰酸铵(NH4CNO)水溶液得到了尿素[CO(NH2)2],尿素[CO(NH2)2]属于( )
| A. | 复合肥料 | B. | 氮肥 | C. | 磷肥 | D. | 钾肥 |
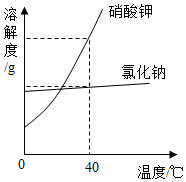 如图是硝酸钾和氯化钾的溶解度曲线.
如图是硝酸钾和氯化钾的溶解度曲线.