题目内容
100g某一定质量分数的稀硫酸恰好与13g锌完全反应.请计算:
(1)反应产生氢气的质量是 g.
(2)稀硫酸中溶质的质量分数.(写出计算过程).
| (1)由消耗的锌的质量可以计算出生成的氢气的质量; (2)由消耗的锌的质量结合锌与硫酸反应的化学方程式来计算出反应的硫酸的质量,进而计算出稀硫酸的质量分数. | |
| 解答: | 解 Zn+H2SO4═ZnSO4+H2↑ 65 98 2 13g y x
解得:x=0.4g,y=19.6g (2)稀硫酸中溶质的质量分数为 答:(2)稀硫酸中溶质的质量分数为19.6%. 故答案为:(1)0.4; (2)19.6%. |

(1)下列实验操作中不正确的是
①制备气体前检查装置的气密性②加热实验结束时,用嘴吹灭酒精灯.
③将用剩的药品放回原试剂瓶中④稀释浓硫酸时,将浓硫酸沿器壁缓慢注入水中.
(2)在实验室里,可用浓盐酸与二氧化锰在加热条件下起反应制取氯气(Cl2),该气体能溶于水,则制取氯气应选择的发生装置和收集装置分别是

(3)某兴趣小组设计的趣味小实验装置如右图所示,其中A、B为未膨胀的气球,C为玻璃导管,D为胶头滴管.用气密性良好的该装置分别进行甲、乙两组实验.实验时均把胶头滴管中的溶液(足量)加入到锥形瓶中,并轻轻振荡.请填写下表中的空白:

| 锥形瓶中的物质 | 胶头滴管中的物质 | 观察到气球(A、B)的变化 | 有关反应的化学方程式 | |
| 甲 | 二氧化碳 | 浓氢氧化钠溶液 | ||
| 乙 | A气球胀大 B气球无明显变化 |
| 实验次数 | 稀盐酸的用量(g) | 剩余固体的质量(g) |
| ① | 20 | 16.25 |
| ② | 40 | 12.50 |
| ③ | 60 | M |
| ④ | 80 | 5.00 |
| ⑤ | 100 | 5.00 |
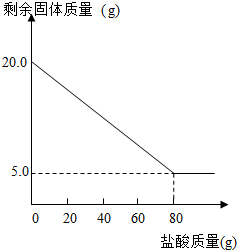
请细心观查表格和图象,回答下列问题:
(1)涉及反应的化学方程式为
(2)第
(3)该石灰石样品中碳酸钙的质量分数为
(4)表格中m=
(5)该样品完全反应生成二氧化碳的质量是
(14分)某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究。
【产品原理】
该厂采用“侯氏制碱法”生产化工产品——纯碱(Na2CO3)和化肥NH4Cl。
生产原理是:将NH3和CO2通入饱和食盐水中得到NaHCO3晶体和NH4Cl溶液,反应的化学方程式为: ;后分离出NaHCO3,加热制得纯碱。
【生产流程】

|
⑴ NH4Cl NH3↑+HCl↑
⑵ 已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解的气体体积)
|
物质 |
NaCl |
NaHCO3 |
NH4Cl |
NH3 |
CO2 |
|
溶解度 |
36.0g |
9.6g |
37.2g |
710 |
0.9 |
【问题讨论】
⑴操作Ⅰ、Ⅱ中,相同操作的名称为 。反应①中发生了两个反应,写出其中一个化学方程式: ,反应①加适量的盐酸,适量是指 。
⑵检验挥发性气体C的方法 。
⑶上述生产流程中可循环使用的是 (填序号)。
A.挥发性气体C B.溶液D C.氢氧化镁 D.化肥NH4Cl
【组成确定】
⑴ 称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
⑵ 另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀。由上述实验可确定纯碱样品含有杂质 (写化学式)。
【含量测定】
|
|
实验一 |
实验二 |
实验三 |
实验四 |
|
固体混合物溶液质量 |
100g |
100g |
100g |
100g |
|
加入CaCl2溶液质量 |
10g |
20g |
30g |
40g |
|
生成的沉淀的质量 |
4g |
m |
10g |
10g |
称取该纯碱样品44 g固体混合物,加水配成400g溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见表:
请分析表中数据回答并计算:
⑴m= g;
⑵在实验三中,完全反应后所得溶液中溶质氯化钠的质量分数是多少?(要求写计算过程,结果保留0.1%)
【总结反思】
请通过计算并结合下表判断此纯碱样品等级为 品,在上述纯碱含量测定中,将CaCl2溶液改为BaCl2溶液,测定误差会减小。
 某兴趣小组的同学为测定某石灰石中碳酸钙(假设:石灰石中的杂质不与盐酸反应)的质量分数,称取一定质量的石灰石置于烧杯中,用某浓度的稀盐酸100g,分5次加入,每次充分反应后,取出固体,经过滤、洗涤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
某兴趣小组的同学为测定某石灰石中碳酸钙(假设:石灰石中的杂质不与盐酸反应)的质量分数,称取一定质量的石灰石置于烧杯中,用某浓度的稀盐酸100g,分5次加入,每次充分反应后,取出固体,经过滤、洗涤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:| 实验次数 | 稀盐酸的用量(g) | 剩余固体的质量(g) |
| ① | 20 | 16.25 |
| ② | 40 | 12.50 |
| ③ | 60 | m |
| ④ | 80 | 5.00 |
| ⑤ | 100 | n |
(1)第______次石灰石中的碳酸钙与盐酸恰好反应完毕.
(2)表格中m=______g,n=______g.
(3)计算该石灰石样品中碳酸钙的质量分数.
(4)计算该石灰石样品完全反应生成二氧化碳的质量.
 :(1)设生成氢气的质量为x,稀硫酸中硫酸的质量为y
:(1)设生成氢气的质量为x,稀硫酸中硫酸的质量为y
 ×100%=19.6%
×100%=19.6% 某兴趣小组的同学为测定某石灰石中碳酸钙(假设:石灰石中的杂质不与盐酸反应)的质量分数,称取一定质量的石灰石置于烧杯中,用某浓度的稀盐酸100g,分5次加入,每次充分反应后,取出固体,经过滤、洗涤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
某兴趣小组的同学为测定某石灰石中碳酸钙(假设:石灰石中的杂质不与盐酸反应)的质量分数,称取一定质量的石灰石置于烧杯中,用某浓度的稀盐酸100g,分5次加入,每次充分反应后,取出固体,经过滤、洗涤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下: