题目内容
5.请用所学过的化学知识填空:(1)托盘天平是实验中常用的仪器,有人按右物左码称得10.2g药品(1g以下用游码),则他所称药品的实际质量为9.8g.
(2)酚酞是一种常用的化学试剂,化学式(分子式)为C20H14O4,每个酚酞分子中共有38个原子,酚酞中碳、氢、氧元素的质量比为120:7:32.
(3)我国使用“长征3号甲”运载火箭的动力由高氯酸铵(NH4ClO4)分解所提供,其反应的化学方程式为2NH4ClO4 $\frac{\underline{\;△\;}}{\;}$N2↑+Cl2↑+4X↑+2O2↑,则X的化学式为H2O.
(4)物质着火燃烧一般需同时满足三个条件:而灭火主要有三种方法:①将可燃物撤离燃烧区,与火源隔离;②将燃着的可燃物与空气隔绝;③使用大量的冷却剂(如水、干冰等),让可燃物的温度降到着火点以下,当你被困在火灾区时,要冷静自救,用湿毛巾或口罩捂住口鼻低身贴墙逃离.
(5)钢铁是重要的金属材料,工业上采用高炉炼铁,请写出炼铁过程中CO和Fe2O3反应的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
分析 (1)根据天平的使用方法是左物右码,左盘的质量等于右盘的质量加游码的质量,即药品质量=砝码质量+游码质量,如果位置放反,根据左盘的质量=右盘的质量+游码的质量,列等式进行计算;
(2)根据标在元素符号右下角的数字表示一个分子中所含原子的个数进行解答;根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
(3)根据化学反应为2NH4ClO4$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+Cl2↑+4X↑+2O2↑,利用质量守恒定律来分析解答X的化学式;(4)根据灭火原理进行分析解答;
(5)根据CO和Fe2O3反应生成铁与二氧化碳进行分析解答.
解答 解:(1)由左盘的质量=右盘的质量+游码的质量可知:砝码质量=药品质量+游码的质量,所以药品质量=砝码质量-游码质量,即药品质量=1.0g-0.2g=9.8g;
(2)酚酞的一个分子是由20个碳原子、14个氢原子和4个氧原子构成的,则酚酞的一个分子里含38个原子;酚酞中碳、氢、氧元素的质量比为(12×20):(1×14):(16×4)=120:7:32;
(3)由化学反应方程式2NH4ClO4$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+Cl2↑+4X↑+2O2↑可知,
反应前后的元素的种类和原子个数应相等,反应前有N、H、Cl、O四种元素,则X中含有H元素,反应前后N、Cl的原子个数相等,而H、O原子的个数不等,由反应前共8个H原子、8个O原子,则反应后应共8个H原子、8个O原子,氧气分子中有O原子,即X中共有8个H原子,4个O原子,再根据X的化学计量数为4,则X的化学式为H2O;
(4)物质着火燃烧一般需同时满足三个条件:而灭火主要有三种方法:①将可燃物撤离燃烧区,与火源隔离;②将燃着的可燃物与空气隔绝;③使用大量的冷却剂(如水、干冰等),让可燃物的温度降到着火点以下,当你被困在火灾区时,要冷静自救,用湿毛巾或口罩捂住口鼻低身贴墙逃离;
(5)钢铁是重要的金属材料,工业上采用高炉炼铁,CO和Fe2O3反应生成铁与二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故答案为:(1)9.8;(2)38;120:7:32;(3)H2O;(4)空气;着火点;(5)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 本题考查的知识点解答,综合性较强,要注意平时知识的积累.

| A. | 碳在空气中燃烧生成二氧化碳 | B. | 电解水 | ||
| C. | 葡萄糖与氧气在酶的作用下反应 | D. | 用过氧化氢反应制氧气 |
| A. | 有能量变化 | B. | 有新物质生成 | ||
| C. | 物质的颜色和状态发生改变 | D. | 有气体或沉淀产生 |

| A. | 镁条 | B. | 碳酸钙 | C. | 硝酸铵 | D. | 氯化钠 |
 ”“
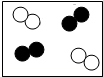
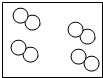
”“ ”分别表示两种不同质子数的原子其中表示化合物的是( )
”分别表示两种不同质子数的原子其中表示化合物的是( )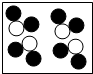

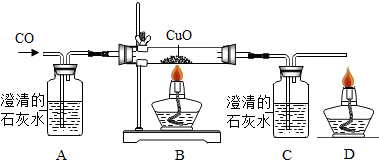 甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.
甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.