题目内容
正常情况下人的胃液pH为0.8~1.5,相应含HCl的溶质质量分数为0.2%~0.4%,胃液中HCl过多与过少都不利于人体健康.某人出现反胃、吐酸水的症状,经检查其胃液中HCl的质量分数为1.49%(胃液密度约为1g/cm3).
(1)正常情况下,人的胃液显 性.
(2)人的胃液总量为100mL,正常人胃液中HCl的质量范围是 g.
(3)服用碱性药品可以治疗胃液中HCl含量过多,你认为该患者 (填“能”或“不能”)服用氢氧化钠来治疗胃液中过多,理由是 .
(4)医生给患者开的药品为胃舒平[有效成分是Al(OH)3],每片胃舒平平含Al(OH)3的质量为0.39g.请根据化学方程式计算该患者至少服用多少片的胃舒平,胃液才能恢复正常?(请写出计算过程)
(1)正常情况下,人的胃液显
(2)人的胃液总量为100mL,正常人胃液中HCl的质量范围是
(3)服用碱性药品可以治疗胃液中HCl含量过多,你认为该患者
(4)医生给患者开的药品为胃舒平[有效成分是Al(OH)3],每片胃舒平平含Al(OH)3的质量为0.39g.请根据化学方程式计算该患者至少服用多少片的胃舒平,胃液才能恢复正常?(请写出计算过程)
考点:酸的化学性质,有关溶质质量分数的简单计算,根据化学反应方程式的计算
专题:常见的酸 酸的通性
分析:(1)根据胃液中含有盐酸,盐酸呈酸性进行解答;
(2)根据溶质的质量分数=
×100%,结合题干给出的信息进行解答;
(3)根据氢氧化钠有很强的腐蚀性进行解答;
(4)首先计算出需要消耗的盐酸质量,根据根据化学方程式求出消耗这些盐酸所需要的氢氧化铝的质量,然后根据每片胃舒平中氢氧化铝的质量求出服用片数.
(2)根据溶质的质量分数=
| 溶质的质量 |
| 溶液的质量 |
(3)根据氢氧化钠有很强的腐蚀性进行解答;
(4)首先计算出需要消耗的盐酸质量,根据根据化学方程式求出消耗这些盐酸所需要的氢氧化铝的质量,然后根据每片胃舒平中氢氧化铝的质量求出服用片数.
解答:解:
1ml=1g/cm3
(1)因胃液中含有盐酸,盐酸呈酸性,故正常情况下,人的胃液显酸性;
(2)根据溶质的质量分数=
×100%,故溶质的质量=溶液质量×溶质的质量分数,100ml×1g/cm3×0.2%=0.2g,
100ml×1g/cm3×0.4%=0.4g,故胃液中HCl的质量范围是:0.2g~0.4g;
(3)因为氢氧化钠有很强的腐蚀性,故不能用氢氧化钠来中和胃酸.
(4)该患者胃液中至少多出HCl的质量为:100ml×1g/cm3×1.49%-0.4g=1.09g
设要使该患者恢复正常,至少需要消耗氢氧化铝的质量为x
Al(OH)3+3HCl═AlCl3+3H2O
78 109.5
x 1.09g
x=0.78g
至少服用胃舒平的片数为
=2
答:该患者至少服用2片的胃舒平,胃液才能恢复正常.
答案:
(1)酸;
(2)0.2~0.4;
(3)不能;氢氧化钠有很强的腐蚀性;
(4)2片
1ml=1g/cm3
(1)因胃液中含有盐酸,盐酸呈酸性,故正常情况下,人的胃液显酸性;
(2)根据溶质的质量分数=
| 溶质的质量 |
| 溶液的质量 |
100ml×1g/cm3×0.4%=0.4g,故胃液中HCl的质量范围是:0.2g~0.4g;
(3)因为氢氧化钠有很强的腐蚀性,故不能用氢氧化钠来中和胃酸.
(4)该患者胃液中至少多出HCl的质量为:100ml×1g/cm3×1.49%-0.4g=1.09g
设要使该患者恢复正常,至少需要消耗氢氧化铝的质量为x
Al(OH)3+3HCl═AlCl3+3H2O
78 109.5
x 1.09g
| 78 |
| 109.5 |
x=0.78g
至少服用胃舒平的片数为
| 0.79g |
| 0.39g |
答:该患者至少服用2片的胃舒平,胃液才能恢复正常.
答案:
(1)酸;
(2)0.2~0.4;
(3)不能;氢氧化钠有很强的腐蚀性;
(4)2片
点评:本题通过治疗胃酸的知识来考查学生化学方程式的计算,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等,认真地选择或解答,并要求熟记质量分数的计算.

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
“金银铜铁锡”俗称五金.在这五种金属中,化学性质最不活泼的金属是( )
| A、金 | B、铜 | C、铁 | D、锡 |
以下所列化肥属于复合肥料的是( )
| A、碳酸氢铵(NH4HCO3) |
| B、硫酸钾 (K2 SO4) |
| C、磷酸二氢铵( NH4H2PO4) |
| D、尿素(CO(NH2)2) |

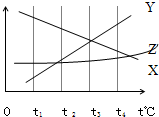 图是X、Y、Z三种物质的溶解度曲线,根据图示回答下列问题:
图是X、Y、Z三种物质的溶解度曲线,根据图示回答下列问题: 做菜用的一种嫩肉粉其主要成分是碳酸氢钠,可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋(含醋酸)等调料烧煮时会产生大量气泡.他对此颇感兴趣,决定对其进行探究.
做菜用的一种嫩肉粉其主要成分是碳酸氢钠,可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋(含醋酸)等调料烧煮时会产生大量气泡.他对此颇感兴趣,决定对其进行探究.