题目内容
 (2012?集美区质检)某化学兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,进行了如下实验.
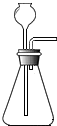
(2012?集美区质检)某化学兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,进行了如下实验.如图所示装置,在锥形瓶中加入1.5g 二氧化锰,从长颈漏斗注入35.0g过氧化氢溶液.当锥形瓶内的物质完全反应后,称量、计算,得出锥形瓶内剩余物的质量为34.9g.
请根据以上信息,计算出该过氧化氢溶液中溶质的质量分数.(最后结果保留一位小数)2H2O2
| ||
分析:在二氧化锰催化下,过氧化氢分解生成水和氧气,由于氧气放出而使锥形瓶内剩余物质量减轻,因此可根据质量守恒定律计算出完全反应所放出氧气的质量;根据反应的化学方程式,由放出氧气的质量计算过氧化氢的质量,然后利用过氧化氢的质量与过氧化氢溶液的质量比,求得溶液中溶质的质量分数.
解答:解:以题意可知该反应生成的氧气的质量是(35.0g+1.5g)-34.9g=1.6g
设34.0g过氧化氢溶液中含有过氧化氢的质量为x
2H2O2
2H2O+O2↑
68 32
x 1.6g
=
x=3.4g
该过氧化氢溶液中溶质的质量分数=
×100%=9.7%
答:该过氧化氢溶液中溶质的质量分数为9.7%.
设34.0g过氧化氢溶液中含有过氧化氢的质量为x
2H2O2
| ||
68 32
x 1.6g
| 68 |
| x |
| 32 |
| 1.6g |
x=3.4g
该过氧化氢溶液中溶质的质量分数=
| 3.4g |
| 35g |
答:该过氧化氢溶液中溶质的质量分数为9.7%.
点评:此题是对化学方程式的计算考查,解题的关键是利用质量守恒定律求出生成的氧气的质量;

练习册系列答案
相关题目
 (2012?集美区质检)化学与生活息息相关
(2012?集美区质检)化学与生活息息相关 (2012?集美区质检)“空瓶生烟”(如图1所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.
(2012?集美区质检)“空瓶生烟”(如图1所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟. ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用如图2表示:该反应的化学方程式为
”表示氯原子,上述反应过程可用如图2表示:该反应的化学方程式为