题目内容
实验室用10g高锰酸钾放在试管里加热,一段时间后,称得剩余固体的质量是9.2g,则剩余物质是( )
| A、K2MnO4和MnO2 |
| B、K2MnO4 |
| C、KMnO4和K2MnO4 |
| D、KMnO4和K2MnO4和MnO2 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;
通过计算10g高锰酸钾完全分解生成氧气的质量,可以判断剩余固体的组成.
通过计算10g高锰酸钾完全分解生成氧气的质量,可以判断剩余固体的组成.
解答:解:设10g高锰酸钾完全分解生成氧气的质量为x,
2KMnO4
K2MnO4+MnO2+O2↑,
316 32
10g x
=
,
x=1.01g,
用10g高锰酸钾放在试管里加热,一段时间后,称得剩余固体的质量是9.2g,则生成氧气的质量为:10g-9.2g=0.8g,
根据计算结果可知,高锰酸钾没有完全分解,则剩余固体物质中含有高锰酸钾、锰酸钾和二氧化锰.
故选:D.
2KMnO4
| ||
316 32
10g x
| 316 |
| 10g |
| 32 |
| x |
x=1.01g,
用10g高锰酸钾放在试管里加热,一段时间后,称得剩余固体的质量是9.2g,则生成氧气的质量为:10g-9.2g=0.8g,
根据计算结果可知,高锰酸钾没有完全分解,则剩余固体物质中含有高锰酸钾、锰酸钾和二氧化锰.
故选:D.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
相关题目
pH=0的溶液是( )
| A、酸性溶液 | B、不存在 |
| C、碱性溶液 | D、中性溶液 |
小明要称10.8克的食盐,他在左边的托盘上装了10克的砝码,游码移至0.8刻度,然后在右边装食盐至两变平衡,实际小明所称食盐的质量是( )
| A、10.8克 | B、10克 |
| C、9.2克 | D、11.6克 |
物质的特性决定物质的用途,你认为下列物质的用途是利用物质物理性质的是( )
| A、铝用于制造电线和电缆 |
| B、氧气用于炼钢 |
| C、氮气充当保护气使用 |
| D、氮气用于生产化肥 |
SO2是污染大气的主要有害物质之一,是形成酸雨的“罪魁祸首”.SO2不属于( )
| A、化合物 | B、混合物 |
| C、氧化物 | D、纯净物 |
具备基本的化学实验技能是进行科学实验探究活动的基础和保证.下列实验操作中,错误的是( )
A、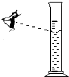 读取液体体积 |
B、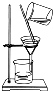 过滤 |
C、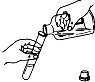 倾倒液体 |
D、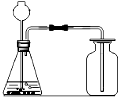 制取二氧化碳 |