题目内容
某化学兴趣小组以“化学反应中,反应物与生成物的质量关系”为课题进行实验探究.相关实验记录如下:
| 数据记录 | 实验一 | 实验二 |
| 反应容器 | 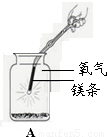 | 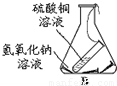 |
| 反应前(g) | 4.8 | 118.4 |
| 反应后(g) | 8.0 | 118.4 |
| 实验结论 | 在化学反应中,生成物的总质量与反应物的总质量不相等 | 在化学反应中,生成物的总质量与反应物的总质量相等 |
(2)你认为实验______(填“实验一”或“实验二”)正确地反映了“化学反应中,反应物和生成物之间的质量关系”.请你分析导致另一个实验结论错误的原因是______;
可见,用实验来研究“化学反应中反应物和生成物之间的质量关系”时,必须在______容器中进行.
(3)请从原子的角度简要分析你认为正确的结论的原因______.
(4)你认为这条科学结论的获得对化学研究的重大意义是______.
【答案】分析:本题考查的是质量守恒定律,必须用到的仪器是托盘天平;其内容是:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和.本题中的实验探究也应符合这一规律,如果用的药品相互反应生成的是沉淀和水,可以用烧杯等敞口容器;如果用的药品生成的是气体、或有气体加入或与空气中的其它成分反应,就必须用密闭的容器.在化学反应中,从微观上原子种类、原子数目和原子的质量都不变;从宏观上元素种类和物质的总质量不变;一定改变的是分子的种类或物质的种类.
解答:解:(1)化学反应中,反应物与生成物的质量关系必须用托盘天平,故答案为:托盘天平
(2)实验二正确地反映了“化学反应中,反应物和生成物之间的质量关系”;实验一中,镁条与氧气反应是在敞口的容器中,应该的密闭容器中进行.故答案为:实验二;镁条与氧气反应是在敞口的容器中进行,空气中的部分氧气会参与反应,导致质量变大,实验失败;密闭;
(3)在化学反应中,从微观上原子种类、原子数目和原子的质量都不变,故答案为:原子种类、原子数目和原子的质量想化学反应前后都不变
(4)质量守恒定律,使人们对化学进行定量的研究有重要的意义,故答案为:使人们对化学进行定量的研究有重要的意义
点评:本考点是有关质量守恒定律的实验探究,要抓住要点:五个一定不变,一个一定变.有关质量守恒定律的考题在中考中经常出现,还要注意药品的选择和装置的选择,本考点经常出现在实验题中.
解答:解:(1)化学反应中,反应物与生成物的质量关系必须用托盘天平,故答案为:托盘天平
(2)实验二正确地反映了“化学反应中,反应物和生成物之间的质量关系”;实验一中,镁条与氧气反应是在敞口的容器中,应该的密闭容器中进行.故答案为:实验二;镁条与氧气反应是在敞口的容器中进行,空气中的部分氧气会参与反应,导致质量变大,实验失败;密闭;
(3)在化学反应中,从微观上原子种类、原子数目和原子的质量都不变,故答案为:原子种类、原子数目和原子的质量想化学反应前后都不变
(4)质量守恒定律,使人们对化学进行定量的研究有重要的意义,故答案为:使人们对化学进行定量的研究有重要的意义
点评:本考点是有关质量守恒定律的实验探究,要抓住要点:五个一定不变,一个一定变.有关质量守恒定律的考题在中考中经常出现,还要注意药品的选择和装置的选择,本考点经常出现在实验题中.

练习册系列答案
相关题目
某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
探究l:研究常见的物质---氢氧化钠和盐酸的反应程度.
探究2:研究酸的性质--硫酸、盐酸和锌反应
通过探究实验,同学们发现硫酸和盐酸溶液都可以和锌反应产生氢气.产生这种共同现象的原因为______
探究3:探索未知---浓硝酸和铜制取气体.
已知Cu+4HN03(浓)=Cu( NO3)2+H2O+2N02↑.N02能和水反应生成硝酸和N0.NO和NO2都是空气的污染物.
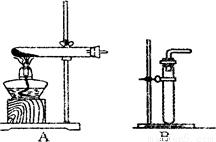
(1)利用该反应制取二氧化氮的发生装置,应选用图所示装置中的______.收集N02的方法为______.
(2)反应NO+X→N02中,X的化学式应为______;若用浓硝酸和铜制取NO,应采用的收集方法是______.
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入l0g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009.8g,请你计算所加碳酸钠溶液的溶质质量分数?
探究l:研究常见的物质---氢氧化钠和盐酸的反应程度.
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入 固体化台物______. | ______ | 盐酸过量 |
通过探究实验,同学们发现硫酸和盐酸溶液都可以和锌反应产生氢气.产生这种共同现象的原因为______
探究3:探索未知---浓硝酸和铜制取气体.
已知Cu+4HN03(浓)=Cu( NO3)2+H2O+2N02↑.N02能和水反应生成硝酸和N0.NO和NO2都是空气的污染物.
(1)利用该反应制取二氧化氮的发生装置,应选用图所示装置中的______.收集N02的方法为______.
(2)反应NO+X→N02中,X的化学式应为______;若用浓硝酸和铜制取NO,应采用的收集方法是______.
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入l0g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009.8g,请你计算所加碳酸钠溶液的溶质质量分数?

 (2013?许昌一模)某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
(2013?许昌一模)某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.

 以尿素[化学式:CO(NH2)2]为反应物,硅胶为催化剂,在380℃~400℃的温度下,反应得到三聚氰胺,同时生产两种无色气体,其中一种气体具有刺激气味.
以尿素[化学式:CO(NH2)2]为反应物,硅胶为催化剂,在380℃~400℃的温度下,反应得到三聚氰胺,同时生产两种无色气体,其中一种气体具有刺激气味. 2)NO2为红棕色气体.(3)氨气是碱性气体,极易溶于水,能与硫酸化合成硫酸铵,对人体有毒害作用.
2)NO2为红棕色气体.(3)氨气是碱性气体,极易溶于水,能与硫酸化合成硫酸铵,对人体有毒害作用. 二氧化碳和氨气;③二氧化碳和二氧化氮……
二氧化碳和氨气;③二氧化碳和二氧化氮…… 猜想.
猜想. 【实验现象和分析】A装置的作用是使生成的三聚氰胺迅速凝华而与气体分离.
【实验现象和分析】A装置的作用是使生成的三聚氰胺迅速凝华而与气体分离.