题目内容
将铁片分别投入下列溶液中,整个溶液质量减少的是( )
| A、硫酸铜 | B、稀硫酸 |
| C、硫酸亚铁 | D、稀盐酸 |
考点:金属的化学性质
专题:金属与金属材料
分析:根据物质间的反应进行分析,金属与酸反应金属溶于酸而使溶液质量增加,金属与盐溶液反应溶液质量的变化取决于参加反应的金属的质量和反应后置换出的金属的质量,若参加反应的金属的质量大于生成的金属的质量,则溶液质量增加,结合题中的选项进行分析解答.
解答:解:A、铁的金属活动性比铜强,所以铁与硫酸铜反应生产硫酸亚铁和铜,
Fe+CuSO4═FeSO4+Cu
56 64
参加反应的铁的质量小于生成的铜的质量,所以溶液质量减小,故A正确;
B、铁与稀硫酸能反应,生成氢气和硫酸亚铁而使溶液质量增加,其原因是:由反应的化学方程式:Fe+H2SO4=FeSO4+H2↑,可知56gFe反应溶液增加(56-2)=54g,所以溶液质量增加,故B错误;
C、铁与硫酸亚铁不能反应,所以溶液质量不会变化,故C错误;
D、铁与稀盐酸能反应,生成氢气和氯化亚铁而使溶液质量增加,其原因是:由反应的化学方程式:Fe+2HCl═FeCl2+H2↑,可知56gFe反应溶液增加(56-2)=54g,所以溶液质量增加,故D错误;
故选:A.
Fe+CuSO4═FeSO4+Cu
56 64
参加反应的铁的质量小于生成的铜的质量,所以溶液质量减小,故A正确;
B、铁与稀硫酸能反应,生成氢气和硫酸亚铁而使溶液质量增加,其原因是:由反应的化学方程式:Fe+H2SO4=FeSO4+H2↑,可知56gFe反应溶液增加(56-2)=54g,所以溶液质量增加,故B错误;
C、铁与硫酸亚铁不能反应,所以溶液质量不会变化,故C错误;
D、铁与稀盐酸能反应,生成氢气和氯化亚铁而使溶液质量增加,其原因是:由反应的化学方程式:Fe+2HCl═FeCl2+H2↑,可知56gFe反应溶液增加(56-2)=54g,所以溶液质量增加,故D错误;
故选:A.
点评:本题考查了金属与酸或盐反应时溶液质量的变化,完成此题,可以依据物质间反应的化学方程式进行计算.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案
相关题目
下列曲线图与实验事实不一致的是( )
A、 在饱和氢氧化钙溶液中加入一定量生石灰后,恢复至室温,整过过程中溶质的质量变化 |
B、 等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量M与反应时间的关系图 |
C、 向一定量氢氧化钾和硝酸钡的混合溶液中,逐滴滴加稀硫酸 |
D、 加热高锰酸钾制氧气,剩余固体中锰元素的质量分数 |
“墙内桃花墙外香”说明了( )
| A、分子之间有间隔 |
| B、分子在不停的运动 |
| C、分子变大了 |
| D、分子很小 |
运送“神州5号”载人飞船的是长征二号F捆绑式大推力运载火箭,升空时的主要燃料之一是偏二甲肼(分子式为C2H8N2).下列有关偏二甲肼组成的叙述,正确的是( )
| A、由2个碳原子、8个氢原子、2个氮原子构成 |
| B、由碳、氢、氮三个元素组成 |
| C、碳、氢、氮的原子个数比为6:2:7 |
| D、碳、氢、氮元素的质量比为6:2:7 |
装有石灰水的试剂瓶时间久了,内壁常附有一层白膜,洗去这层白膜的最好方法是( )
| A、用水洗 |
| B、用盐水清洗 |
| C、先用盐酸洗再用水洗 |
| D、先用氢氧化钠溶液洗再用水洗 |
下列各组元素的原子结构示意图中,具有相似化学性质的一组元素是( )
A、 |
B、 |
C、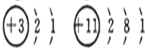 |
D、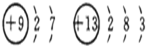 |