题目内容
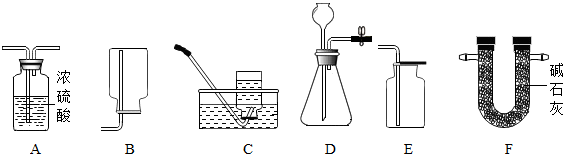
14.小敏同学想用废弃的黄铜屑(Cu-Zn合金)和稀硫酸制取氢气用100g质量分数为98%的浓硫酸稀释成20%的稀硫酸,她应选择的操作是B(填字母)理由是③(填序号),应加入水的体积是390mL.
①浓硫酸具有吸水性 ②水的密度比浓硫酸小 ③浓硫酸溶于水放热
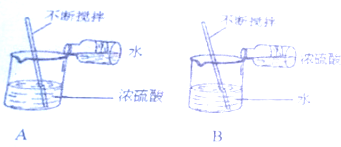
分析 浓硫酸的稀释从理论上来说,是指将浓硫酸加水变成稀硫酸的过程,但由于水的密度较小,浮在浓硫酸上面,而浓硫酸溶于水时会放出大量的热,使水立刻沸腾,造成硫酸液滴向四周飞溅,这是非常危险的.因此,浓硫酸稀释时,一定要浓硫酸沿器壁慢慢注入水里,并不断用玻璃棒搅拌;切不可将水倒进浓硫酸里.
向浓溶液加水稀释前后溶液中溶质的质量不变,利用浓溶液中溶质的质量可计算加水稀释时水的质量.
解答 解:由于水的密度较小,浮在浓硫酸上面,而浓硫酸溶于水时会放出大量的热,使水立刻沸腾,造成硫酸液滴向四周飞溅,所以浓硫酸稀释时,一定要浓硫酸沿器壁慢慢注入水里,并不断用玻璃棒搅拌.
设需增加水的质量为x
100g×98%=(100g+x)×20%
x=390g
390g合390mL.
故答案是:B;③;390.
点评 在进行浓硫酸稀释时,切不可把水倒入浓硫酸中,防止液体受热不匀而溅出.

练习册系列答案
相关题目
4.下列物质由离子构成的是( )
| A. | 硫酸铜 | B. | 氧气 | C. | 金刚石 | D. | 汞 |
5.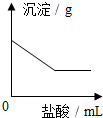 有一包白色粉末,可能含有BaCl2、K2SO4、Na2CO3、CuSO4中的一种或几种,取样溶液于足量的水,有白色沉淀产生,过滤,滤液呈无色;向沉淀中滴加稀盐酸,沉淀的质量与加入盐酸体积的关系如图所示,由此推断白色粉末的成分是( )
有一包白色粉末,可能含有BaCl2、K2SO4、Na2CO3、CuSO4中的一种或几种,取样溶液于足量的水,有白色沉淀产生,过滤,滤液呈无色;向沉淀中滴加稀盐酸,沉淀的质量与加入盐酸体积的关系如图所示,由此推断白色粉末的成分是( )
 有一包白色粉末,可能含有BaCl2、K2SO4、Na2CO3、CuSO4中的一种或几种,取样溶液于足量的水,有白色沉淀产生,过滤,滤液呈无色;向沉淀中滴加稀盐酸,沉淀的质量与加入盐酸体积的关系如图所示,由此推断白色粉末的成分是( )
有一包白色粉末,可能含有BaCl2、K2SO4、Na2CO3、CuSO4中的一种或几种,取样溶液于足量的水,有白色沉淀产生,过滤,滤液呈无色;向沉淀中滴加稀盐酸,沉淀的质量与加入盐酸体积的关系如图所示,由此推断白色粉末的成分是( )| A. | 可能有K2SO4 | |
| B. | 可能有BaCl2 | |
| C. | 肯定只有Na2CO3 | |
| D. | 肯定有BaCl2、K2SO4、Na2CO3,没有CuSO4 |
2.如图是碳和碳的化合物的转化关系: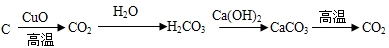
其各步转化的基本反应类型从左到右依次是( )
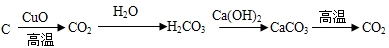
其各步转化的基本反应类型从左到右依次是( )
| A. | 化合、分解、置换、复分解 | B. | 置换、化合、复分解、分解 | ||
| C. | 复分解、化合、置换、分解 | D. | 分解、置换、化合、复分解 |