题目内容
15.许多因素会影响化学反应速率,情分析下列事实,分别说明在其他因素不变时,这些因素是如何影响化学反应速率的.(1)单质硫在纯氧中燃烧比在空气中进行得更快,更剧烈.
(2)同种食品在冬天更容易变质.
(3)过氧化氢在常温下能缓慢分解,加入二氧化锰后分解加速.
(4)相同质量的锌粉和锌粒分别加入足量浓度相等的稀硫酸中,前者先反应完.
分析 可以根据影响化学反应速率的因素方面进行分析、判断,从而得出正确的结论.
解答 解:(1)纯氧中的氧气的浓度大于空气中氧气的浓度,故影响化学反应速率的因素是氧气的浓度,故答案为:氧气的浓度越大,化学反应的速率越大;
(2)温度越高反应的速率越快,同种食品在夏天比冬天更容易变质.故答案为:升高温度,可以加快化学反应速率.
(3)过氧化氢溶液在常温下能缓慢分解,若加入少量Mn02时分解加速.说明化学反应速率受催化剂的影响,故答案为:使用催化剂,可以加快化学反应速率.
(4)在相同质量的锌粉和锌粒中分别加入足量10%的稀盐酸,前者先反应完.说明反应物的接触面积越大,反应的速率大,故答案为:增大反应物接触面积,可以加快化学反应速率.
点评 解答本题的关键是要充分理解影响化学反应速率的因素,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
6.2015年5月11日,环境保护部向媒体公布的2015年“环境日”主题是“践行绿色生活”,该主题旨在增强全民环境意识、节约意识、生态意识,选择低碳、节俭的绿色生活方式和消费模式,形成人人、事事、时时崇尚生态文明的社会新风尚,为生态文明建设奠定坚实的社会和群众基础.下面做法不符合这一主题的是( )
| A. | 大量使用农药化肥,提高农作物产量 | |
| B. | 工业废水处理达标后排放,防止水体污染 | |
| C. | 限制使用塑料购物袋,减少白色污染 | |
| D. | 推广利用太阳能、风能,缓解温室效应 |
3.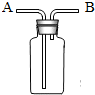 用如图所示装置进行如下实验,能达到实验目的是( )
用如图所示装置进行如下实验,能达到实验目的是( )
 用如图所示装置进行如下实验,能达到实验目的是( )
用如图所示装置进行如下实验,能达到实验目的是( )| A. | 瓶中盛满水,从B口进气,用排水法收集CO2 | |
| B. | 瓶中盛适量碱石灰,从A口进气来干燥HCl | |
| C. | 从B口进气,用排空气法收集CO2 | |
| D. | 瓶中盛满水,A口连导管并伸入量筒中,从B口进气,用排水法测量生成H2的体积 |
20.元素符号“N”可以表示( )
| A. | 氮气的化学式 | B. | 1个氮原子 | ||
| C. | 1个氮元素 | D. | 氮的相对原子质量 |
7.下列物质完全由离子构成的是( )
| A. | 浓硫酸 | B. | 金刚石 | C. | 氧化铁 | D. | 硫酸铜 |
4.铝在氧气中燃烧得到氧化铝,在这个反应中,铝、氧气、氧化铝的质量比为( )
| A. | 108:96:204 | B. | 27:32:108 | C. | 4:3:2 | D. | 54:96:108 |
5.下列实验操作或装置正确的是( )
| A. |  | B. |  | C. |  | D. |  |