题目内容
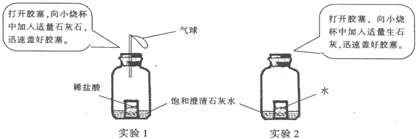
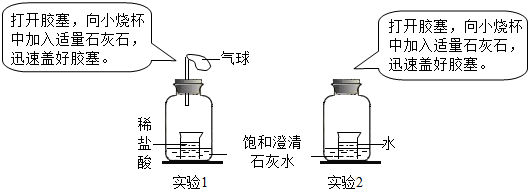
22、某同学做了两个实验:
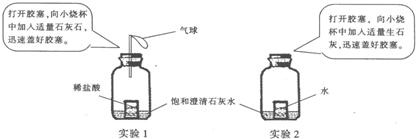
(1)实验l中澄清石灰水出现浑浊,请写出实验l中发生反应的化学方程式:
(2)实验2中澄清石灰水出现浑浊,产生此现象的原因是:

(1)实验l中澄清石灰水出现浑浊,请写出实验l中发生反应的化学方程式:
CaCO3+2HCl═CaCl2+CO2↑+H2O
、Ca(OH)2+CO2═CaCO3↓+H2O
.实验l中,在玻璃管上端固定一个较大的没有充气的气球,目的是:防止瓶内的压强过大,并使生成的CO2与Ca(OH)2充分反应
.(2)实验2中澄清石灰水出现浑浊,产生此现象的原因是:
生石灰与水反应放出大量的热量,使瓶内温度升高,Ca(OH)2的溶解度下降,Ca(OH)2固体析出而出现浑浊
.分析:本题主要考查二氧化碳的制法和性质,并对装置进行了改进.在常温下用石灰石和稀盐酸来制取二氧化碳,因此不需要加热.在瓶口放一个气球是为了防止内外产生压强差.根据学过的知识生石灰和水反应,会放出大量的热,而熟石灰的溶解度随着温度的升高而减小.书写化学方程式时,要注意配平.
解答:解:(1)由实验l中澄清石灰水出现浑浊,我们知道生成的二氧化碳气体与石灰水发生了化学反应.在玻璃管上端固定一个较大的没有充气的气球,是为了防止内外产生压强差,并且使二氧化碳与石灰水充分反应.故答案为:CaCO3+2HCl═CaCl2+CO2↑+H2O;Ca(OH)2+CO2═CaCO3↓+H2O;防止瓶内的压强过大,并使生成的CO2与Ca(OH)2充分反应.
(2)实验2中澄清石灰水出现浑浊,是因为生石灰和水反应会放出大量的热,放出的热量是使的氢氧化钙的溶解度变小,从而析出固体.
故答案为:生石灰与水反应放出大量的热量,使瓶内温度升高,Ca(OH)2的溶解度下降,Ca(OH)2固体析出而出现浑浊.
(2)实验2中澄清石灰水出现浑浊,是因为生石灰和水反应会放出大量的热,放出的热量是使的氢氧化钙的溶解度变小,从而析出固体.
故答案为:生石灰与水反应放出大量的热量,使瓶内温度升高,Ca(OH)2的溶解度下降,Ca(OH)2固体析出而出现浑浊.
点评:本考点主要考查气体的制法和性质,同时也考查了溶解度随温度的变化情况和化学方程式的书写,还考查了化学反应与压强和温度的关系,综合性比较强,是中考的重要考点之一.本考点主要出现在实验题中.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目