题目内容
有一种外观类似黄金的合金(铜和锌的合金),实验室提供一瓶稀硫酸和必要仪器来测量该合金中铜的质量分数.取上述合金粉末40g放入烧杯中,加入足量的稀硫酸50g,并在不同时刻测定烧杯内剩余物质的总质量(如下表).分析表中数据,完成下列问题:
(1)完全反应后,生成氢气的质量为 g.
(2)该合金中铜的质量分数(写出计算过程) .
| 反应时间(分钟) | 1.0 | 1.5 | 2.0 | 2.5 |
| 烧杯内剩余物质的总质量(g) | 89.8 | 89.65 | 89.6 | 89.6 |
(2)该合金中铜的质量分数(写出计算过程)
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气;
反应前后的质量差即为反应生成氢气的质量,根据氢气的质量可以计算锌的质量,进一步可以计算该合金中铜的质量分数.
反应前后的质量差即为反应生成氢气的质量,根据氢气的质量可以计算锌的质量,进一步可以计算该合金中铜的质量分数.
解答:解:(1)完全反应后,生成氢气的质量为:40g+50g-89.6g=0.4g,
故填:0.4;
(2)设锌的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 2
x 0.4g
=
,
x=13g,
该合金中铜的质量分数为:
×100%=67.5%,
故填:67.5%.
故填:0.4;
(2)设锌的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 2
x 0.4g
| 65 |
| x |
| 2 |
| 0.4g |
x=13g,
该合金中铜的质量分数为:
| 40g-13g |
| 40g |
故填:67.5%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目


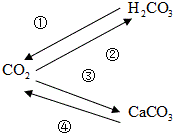 请写出实现下列转化的四个反应的化学方程式:
请写出实现下列转化的四个反应的化学方程式: