题目内容
20.粗盐中含有MgCl2、CaCl2等杂质.提纯粗盐的工艺流程如如图.请回答问题.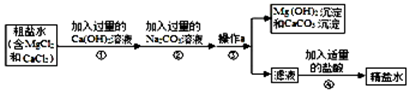
(1)步骤①中发生的化学反应方程式是Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓;
(2)步骤②加入过量的碳酸钠溶液的作用是除去CaCl2和过量的Ca(OH)2;
(3)操作a的名称是过滤;
(4)现有50g质量分数为10%的NaCl溶液.如若将上述溶液稀释为浓度4%NaCl溶液,需要水的质量是75g.
分析 氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;
过滤能够把固体和液体分离;
溶液稀释前后,溶质质量不变.
解答 解:(1)步骤①中氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,发生的化学反应方程式是:Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓.
故填:Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓.
(2)步骤②加入过量的碳酸钠溶液的作用是除去CaCl2和过量的 Ca(OH)2.
故填:除去CaCl2和过量的 Ca(OH)2.
(3)操作a的名称是过滤,通过过滤把沉淀和液体分离.
故填:过滤.
(4)设需要水的质量为x,
根据题意有:50g×10%=(50g+x)×4%,
x=75g,
故填:75.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列物质中属于纯净物的是( )
| A. | 空气中分离出来的稀有气体 | B. | 结冰的蒸馏水 | ||
| C. | 食盐水 | D. | 75%的医用酒精 |
9.用括号内物质不能一次性区别开下列各组物质的是( )
| A. | CaO、CaCO3、KCl 三种固体【水】 | |
| B. | CaCl2、Na2CO3、K2SO4三种溶液【Ba(OH)2溶液】 | |
| C. | Cu、Fe、CuO三种固体【稀盐酸】 | |
| D. | CaCl2、Na NO3、K2CO3三种溶液【Ca(OH)2溶液】 |
10.在Fe2O3中,铁氧元素的质量比为( )
| A. | 2:3 | B. | 3:2 | C. | 7:3 | D. | 21:8 |
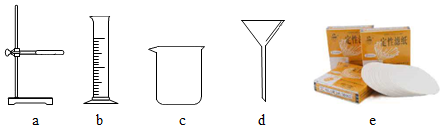
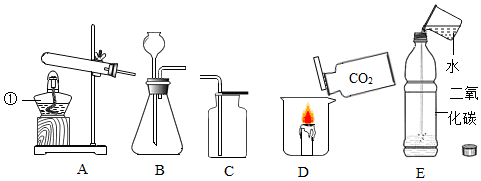
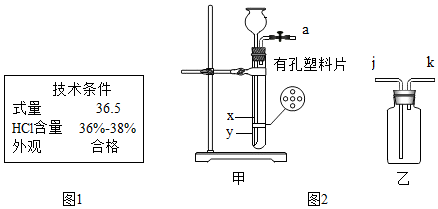 实验室制备二氧化碳的实验如下:
实验室制备二氧化碳的实验如下: